题目内容
16. 常温下,用NaOH溶液滴定20.00mL0.1mol•L-1CH3COOH溶液所得滴定曲线如图,下列说法正确的是( )
常温下,用NaOH溶液滴定20.00mL0.1mol•L-1CH3COOH溶液所得滴定曲线如图,下列说法正确的是( )| A. | 点①所示溶液中:c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+) | |
| B. | 点②所示溶液中:c(Na+)═c(CH3COOH)+c(CH3COO-) | |
| C. | 点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| D. | 滴定过程中不可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
分析 A.①处溶质为醋酸和醋酸钠,溶液呈酸性,则c(H+)>c(OH-),结合电荷守恒、物料守恒判断;
B.②处pH=7,呈中性,则c(OH-)=c(H+),根据电荷守恒分析;
C.③处溶质为醋酸钠,醋酸根离子水解,溶液呈碱性,则c(Na+)>c(CH3COO-)、c(OH-)>c(H+),氢氧根离子浓度较小,则c(CH3COO-)>c(OH-),据此判断离子浓度大小;
D.当滴入的氢氧化钠较少时,溶液呈碱性,此时可满足该关系.
解答 解:A.①溶质为醋酸和醋酸钠,溶液呈酸性,则c(H+)>c(OH-),根据电荷守恒c(CH3COO-)+c(OH-)=c(Na+)+c(H+)可知:c(Na+)>c(CH3COO-),根据物料守恒可知c(Na+)>c(CH3COOH),则c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+),故A正确;
B.②处pH=7,则c(OH-)=c(H+),根据电荷守恒c(CH3COO-)+c(OH-)=c(Na+)+c(H+)可知:c(Na+)=c(CH3COO-),故B错误;
C.③处溶质为醋酸钠,醋酸根离子水解,溶液呈碱性,则c(Na+)>c(CH3COO-)、c(OH-)>c(H+),氢氧根离子浓度较小,则c(CH3COO-)>c(OH-),溶液中离子浓度大小为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故C错误;
D.当滴入的氢氧化钠较少时,溶液呈碱性,此时离子浓度大小可以满足:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-),故D错误;
故选A.
点评 本题考查酸碱混合的定性判断及溶液pH的计算,题目难度不大,明确曲线各点对应溶质组成为解答关键,注意掌握溶液酸碱性与溶液pH的关系,能够利用电荷守恒、物料守恒及盐的水解原理正确平离子浓度大小比较.

| A. | 用加入适量铜粉的方法除去Cu(NO3)2溶液中混有的AgNO3 | |
| B. | 向某无色未知溶液中仅加入BaCl2溶液,以检验未知溶液的SO42- | |
| C. | 用洗气瓶中的NaOH溶液除去CO2中混有的HCl气体 | |
| D. | 先后添加酚酞试液、BaCl2溶液,将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开 |
| A. | 标准状况下,11.2L的水中含有0.5NA个水分子 | |
| B. | 含有1molHCl的盐酸中离子总数为NA个 | |
| C. | 1molO2和H2的混合气体中含有NA个分子 | |
| D. | 1mol大米中含有NA个大米粒子 |
| A. | 15种 | B. | 16种 | C. | 17种 | D. | 18种 |
| A. | 玻璃棒 | B. | 容量瓶 | C. | 漏斗 | D. | 胶头滴管 |
| A. | Si有良好的半导体性能,可用于制备光导纤维 | |
| B. | CO2通入CaCl2溶液中,先有沉淀,后沉淀消失 | |
| C. | 2-氯甲苯的结构简式: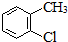 | |
| D. | 取久置的Na2O2粉末,向其中滴加过量的盐酸,产生无色气体,说明Na2O2变质 |
| A. | 溶解度:MgCO3>Mg(OH)2 | B. | 金属性:Mg<K | ||
| C. | 还原性:H2S<SiH4 | D. | 稳定性:HF>PH3 |
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
| A. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | B. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO | ||
| C. | CuO+2HCl═CuCl2+H2O | D. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 |