题目内容
在25mL 0.1 mol·L-1 NaOH溶液中逐滴加入0.2 mol·L-1CH3COOH溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是
A.对于曲线上AB间任一点,溶液中都有:c(Na+) >c(CH3COO-) >c(OH-) >c(H+)
B.在B点,a>12.5,且有c(Na+) = c(CH3COO-) = c(OH-) = c(H+)
C.在C点,c(CH3COO-) -c(Na+) =c(H+) - c(OH-)
D.在D点,c(CH3COO-) + c(CH3COOH)= c(Na+)
C
解析:当加入的醋酸很少时,溶液中c(OH-)可以大于c(CH3COO-)。当醋酸和氢氧化钠恰好反应时,溶液显碱性,此时消耗醋酸的体积是12.5ml。B点显中性,说明醋酸过量,即a>12.5,但c(Na+) = c(CH3COO-) > c(OH-) = c(H+)。C点显酸性,根据电荷守恒可知c(CH3COO-)+ c(OH-) = c(H+)+c(Na+),所以选项C 正确。当加入25ml醋酸时,根据原子守恒可知c(CH3COO-) + c(CH3COOH) =2 c(Na+),所以答案是C。

练习册系列答案
相关题目
 (2010?南京二模)25℃时,下列溶液中微粒的物质的量浓度关系正确的是( )
(2010?南京二模)25℃时,下列溶液中微粒的物质的量浓度关系正确的是( )
 的
的 与
与 混合溶液中:
混合溶液中: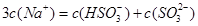
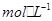 的KHA溶液,其PH=10 c(K+)﹥c(OH-)﹥c(HA-)
的KHA溶液,其PH=10 c(K+)﹥c(OH-)﹥c(HA-)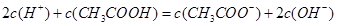
 溶液中逐滴加入0.2
溶液中逐滴加入0.2 溶液,溶液pH变化如右图所示,在A、B间任一点,溶液中一定都存在下列关系:
溶液,溶液pH变化如右图所示,在A、B间任一点,溶液中一定都存在下列关系: