题目内容
4.下列有关实验操作、现象和解释或结论都正确的是( )| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 稀HNO3中加入过量的Fe 粉,充分反应后,滴入KSCN 溶液 | 溶液呈红色 | 稀HNO3将Fe 氧化为Fe3+ |
| B | 某钾盐溶于盐酸,产生无色无味气体,通过澄清石灰水 | 有白色沉淀出现 | 该钾盐是K2CO3 |
| C | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| D | Al 箔插入稀HNO3中 | 无现象 | Al箔表面被HNO3氧化,形成致密了氧化膜 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.稀HNO3中加入过量的Fe 粉,反应生成硝酸亚铁;
B.无色无味气体为二氧化碳;
C.氨水中一水合氨电离出氢氧根离子,显碱性;
D.Al与稀硝酸反应生成NO.
解答 解:A.稀HNO3中加入过量的Fe 粉,反应生成硝酸亚铁,则充分反应后,滴入KSCN 溶液,无现象,故A错误;
B.无色无味气体为二氧化碳,则该钾盐是K2CO3或KHCO3,或二者的混合物,故B错误;
C.氨水中一水合氨电离出氢氧根离子,显碱性,则用玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色,故C正确;
D.Al与稀硝酸反应生成NO,有气泡生成,而Al遇浓硝酸发生钝化,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应与现象、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
2.氯化铁和氯化铜溶于足量水形成的溶液中含有0.8mol氯离子,且溶液中铜元素物质的量为铁元素的一半.现要使原溶液中的金属阳离子都转化为亚铁离子,需加铁粉( )
| A. | 5.6g | B. | 11.2g | C. | 16.8g | D. | 22.4g |
12.工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”.并能以它们为原料生产一系列化工产品.为提高原料的利用率,节能降耗.设计如图1所示工艺流程,其中氯碱工业装置中的电极未标出.
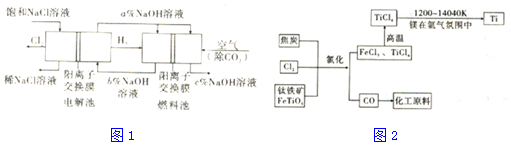
(1)电解饱和食盐水的化学方程式为2Cl-+2H2$\frac{\underline{\;电解\;}}{\;}$2OH-+Cl2↑+H2↑.
(2)为除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,正确的操作步骤的顺序是B (填序号).
①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液
A.①④①②⑤③B.①②⑤④①③C.①②④⑤③D.④②⑤
(3)图中NaOII溶液的质量分数a%、b%、c%,由大到小的顺序为c%>a%>b%.
(4)氯碱工业的产物NaOH与不同物质反应可以生成不同的盐.已知常温下,浓度均为0.1mol/L的四种钠盐溶液pH如表,下列说法不正确的是BD(填序号).
A.向氯水中加入NaHCO3,可以增大氯水中次氯酸的浓度
B.四种溶液中,水的电离程度最大的是NaClO
C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最大的是HClO
D.四种盐的阴离子结合H+能力最强的是HCO3-
(5)若利用电解氯化钠溶液所得的气体制36.5%的浓盐酸100t,最少需要消耗食盐58.5t.
(6)氯碱工业产品Cl2可用于冶炼钛铁矿得到金属钛,流程如图2.写出钛铁矿经氯化法得到四氯化钛的化学方程式:2FeTiO3+6C+7Cl2=2FeCl3+2TiCl4+6CO.
(7)氮气和氩气是两种化学性质相对稳定的气体.镁还原TiCl4的反应中为防止Mg和Ti被氧化选择稀有气体氩气.试用化学反应方程式解释不选用氮气的原因:3Mg+N2$\frac{\underline{\;高温\;}}{\;}$Mg3N2.

(1)电解饱和食盐水的化学方程式为2Cl-+2H2$\frac{\underline{\;电解\;}}{\;}$2OH-+Cl2↑+H2↑.
(2)为除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,正确的操作步骤的顺序是B (填序号).
①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液
A.①④①②⑤③B.①②⑤④①③C.①②④⑤③D.④②⑤
(3)图中NaOII溶液的质量分数a%、b%、c%,由大到小的顺序为c%>a%>b%.
(4)氯碱工业的产物NaOH与不同物质反应可以生成不同的盐.已知常温下,浓度均为0.1mol/L的四种钠盐溶液pH如表,下列说法不正确的是BD(填序号).
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
B.四种溶液中,水的电离程度最大的是NaClO
C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最大的是HClO
D.四种盐的阴离子结合H+能力最强的是HCO3-
(5)若利用电解氯化钠溶液所得的气体制36.5%的浓盐酸100t,最少需要消耗食盐58.5t.
(6)氯碱工业产品Cl2可用于冶炼钛铁矿得到金属钛,流程如图2.写出钛铁矿经氯化法得到四氯化钛的化学方程式:2FeTiO3+6C+7Cl2=2FeCl3+2TiCl4+6CO.
(7)氮气和氩气是两种化学性质相对稳定的气体.镁还原TiCl4的反应中为防止Mg和Ti被氧化选择稀有气体氩气.试用化学反应方程式解释不选用氮气的原因:3Mg+N2$\frac{\underline{\;高温\;}}{\;}$Mg3N2.
19.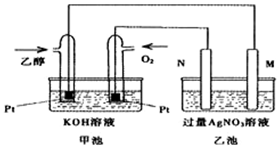 已知甲醇、乙醇都是重要的有机化工原料,回答下列问题:
已知甲醇、乙醇都是重要的有机化工原料,回答下列问题:
(1)图是一个乙醇燃料电池常温工作原理示意图,乙池中的两个电极一个是石墨电极,一个是铁电极.工作时M、N两个电极的质量都不减少,则下列说法正确的是C.
A.M电极的材料是石墨
B.若乙池中某一电极质量增加4.32g时,理论上消耗氧气为448mL
C.在此过程中,甲池中OH-向通乙醇的一极移动
D.在此过程中,乙池溶液中电子从M电极向N电极移动
(2)写出乙醇燃料电池正极的电极反应式O2+2H2O+4e-=4OH-.
(3)已知:甲醇脱水反应 ①2CH3OH(g)=CH3OCH3(g)+H2O(g)?△H1
甲醇制烯烃反应 ②2CH3OH(g)=C2H4 (g)+2H2O(g)?△H2
乙醇异构化反应 ③CH3CH2OH(g)=CH3OCH3(g))?△H3
则乙烯气相直接水合反应C2H4 (g)+H2O(g)=C2H5OH(g)的?△H=△H1-△H2-△H3(用含△H1、△H2、△H3表示).
(4)工业上可利用CO或CO2来生产甲醇.甲醇制备的相关信息如表:
①据表信息推导出K1、K2与K3之间的关系,K3=K1K2用K1、K2表示).
②反应②是吸热反应(选填“吸热”“放热”).
 已知甲醇、乙醇都是重要的有机化工原料,回答下列问题:
已知甲醇、乙醇都是重要的有机化工原料,回答下列问题:(1)图是一个乙醇燃料电池常温工作原理示意图,乙池中的两个电极一个是石墨电极,一个是铁电极.工作时M、N两个电极的质量都不减少,则下列说法正确的是C.
A.M电极的材料是石墨
B.若乙池中某一电极质量增加4.32g时,理论上消耗氧气为448mL
C.在此过程中,甲池中OH-向通乙醇的一极移动
D.在此过程中,乙池溶液中电子从M电极向N电极移动
(2)写出乙醇燃料电池正极的电极反应式O2+2H2O+4e-=4OH-.
(3)已知:甲醇脱水反应 ①2CH3OH(g)=CH3OCH3(g)+H2O(g)?△H1
甲醇制烯烃反应 ②2CH3OH(g)=C2H4 (g)+2H2O(g)?△H2
乙醇异构化反应 ③CH3CH2OH(g)=CH3OCH3(g))?△H3
则乙烯气相直接水合反应C2H4 (g)+H2O(g)=C2H5OH(g)的?△H=△H1-△H2-△H3(用含△H1、△H2、△H3表示).
(4)工业上可利用CO或CO2来生产甲醇.甲醇制备的相关信息如表:
| 化学反应及平衡常数 | 平衡常数数值 | ||
| 500℃ | 800℃ | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?H2O(g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g) | K3 | 2.5 | 0.375 |
②反应②是吸热反应(选填“吸热”“放热”).
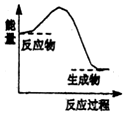
9.下列反应中,属于氧化还原反应且反应前后能量变化如图所示的是( )

| A. | 氢氧化钾与硫酸的反应 | |
| B. | 金属镁与盐酸的反应 | |
| C. | 高温条件下碳粉与二氧化碳的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl固体的反应 |
16. 短周期主族元素X、Y、Z、W的原子序数依次增大.四种元素形成的单质依次为m、n、p、q; r、t、u是这些元素组成的二元化合物,其中u为葡萄酒中抑菌成分;25℃时,0.01mol/L的v溶液中:$\frac{c({H}^{+})}{c(O{H}^{-})}$=1.0×10-10.上述物质的转化关系如图所示.下列说法正确的是( )
短周期主族元素X、Y、Z、W的原子序数依次增大.四种元素形成的单质依次为m、n、p、q; r、t、u是这些元素组成的二元化合物,其中u为葡萄酒中抑菌成分;25℃时,0.01mol/L的v溶液中:$\frac{c({H}^{+})}{c(O{H}^{-})}$=1.0×10-10.上述物质的转化关系如图所示.下列说法正确的是( )
 短周期主族元素X、Y、Z、W的原子序数依次增大.四种元素形成的单质依次为m、n、p、q; r、t、u是这些元素组成的二元化合物,其中u为葡萄酒中抑菌成分;25℃时,0.01mol/L的v溶液中:$\frac{c({H}^{+})}{c(O{H}^{-})}$=1.0×10-10.上述物质的转化关系如图所示.下列说法正确的是( )
短周期主族元素X、Y、Z、W的原子序数依次增大.四种元素形成的单质依次为m、n、p、q; r、t、u是这些元素组成的二元化合物,其中u为葡萄酒中抑菌成分;25℃时,0.01mol/L的v溶液中:$\frac{c({H}^{+})}{c(O{H}^{-})}$=1.0×10-10.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 原子半径的大小:X<Y<Z<W | |
| B. | 元素的非金属性:Y>W>X | |
| C. | t中只含离子键 | |
| D. | v能抑制水的电离而u能促进水的电离 |
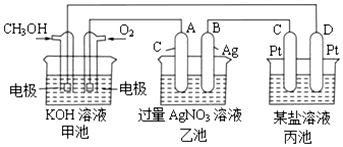
13. 短周期元素W、X、Y、Z的原子序数依次增加.m、n、r是由这些元素组成的化合物,p、q分别是元素W、Z的气体单质.r溶液是实验室中常见试剂,常温下0.1mol•L-1r溶液的pH为13.工业上制备r和q的反应如图.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.m、n、r是由这些元素组成的化合物,p、q分别是元素W、Z的气体单质.r溶液是实验室中常见试剂,常温下0.1mol•L-1r溶液的pH为13.工业上制备r和q的反应如图.下列说法正确的是( )
 短周期元素W、X、Y、Z的原子序数依次增加.m、n、r是由这些元素组成的化合物,p、q分别是元素W、Z的气体单质.r溶液是实验室中常见试剂,常温下0.1mol•L-1r溶液的pH为13.工业上制备r和q的反应如图.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.m、n、r是由这些元素组成的化合物,p、q分别是元素W、Z的气体单质.r溶液是实验室中常见试剂,常温下0.1mol•L-1r溶液的pH为13.工业上制备r和q的反应如图.下列说法正确的是( )| A. | W、与X、Y、Z形成的化合物均是共价化合物 | |
| B. | 简单离子半径:Z>Y>X | |
| C. | X、Y、Z形成的化合物水溶液一定呈碱性 | |
| D. | X、Y形成的化合物一定含有离子键 |
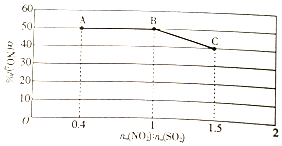 已知NO2与以SO2能发生反应:NO2(g)+SO2(g)?SO3(g)+NO(g).
已知NO2与以SO2能发生反应:NO2(g)+SO2(g)?SO3(g)+NO(g).