题目内容
18.将含3mol Na2CO3的溶液逐滴加入到含2mol MCln的盐溶液中,恰好将溶液中的Mn+离子完全沉淀为碳酸盐,则MCln中n值是( )| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
分析 Na2CO3溶液逐滴加入到MCln盐溶液中,恰好将溶液中的Mn+离子完全沉淀为碳酸盐,同时生成氯化钠,钠离子的物质的量与氯离子的物质的量相等,据此计算n值.
解答 解:将含3mol Na2CO3的溶液逐滴加入到含2mol MCln的盐溶液中,恰好将溶液中的Mn+离子完全沉淀为碳酸盐,同时生成氯化钠,钠离子的物质的量与氯离子的物质的量相等,则:
3mol×2=2mol×n,解得n=3.
故选:C.
点评 本题考查了物质的量的有关计算,难度不大,注意离子反应发生的条件与离子方程式书写,可以根据碳酸根与Mn+离子所带电荷数相等计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列各组变化中,每一转化在一定条件下均能一步实现的是( )


| A. | ①和② | B. | ②和③ | C. | ①和③ | D. | ①②③ |
9.某溶液中含有大量NH4+、Na+、HCO3ˉ、CO32ˉ、CH3COO-,加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)( )
| A. | Na+ | B. | CO32ˉ | C. | CH3COO- | D. | NH4+ |
13.常温下,将a1mLb1mol•L-1CH3COOH溶液加入到a2mLb2mol•L-1NaOH溶液.下列结论中正确的是( )
| A. | 若a1=a2,b1=b2,则混合溶液中c(CH3COO-)=c(Na+)>c(H+)=c(OH-) | |
| B. | 若a1=a2,b1=2b2,则混合溶液中c(CH3COO-)>c(CH3COOH)>c(Na+) | |
| C. | 若a1b1>a2b2,则混合液的pH一定大于7 | |
| D. | a1=a2,且混合溶液的pH<7,则b1一定大于b2 |
3.下列有关仪器的使用正确的是( )
| A. | 将固体药品放在蒸发皿中进行高温焙烧 | |
| B. | 配制480mLNaOH溶液需要的主要仪器有480mL容量瓶、玻璃棒、烧杯、量筒等 | |
| C. | 向试管中滴加液体时胶头滴管一定应悬于试管口的正上方 | |
| D. | 冷凝管中冷却水的流向一定是下口进水、上口出水 |
13.在无色透明的强酸性溶液中,下列各组离子能大量共存的是( )
| A. | NO3-、Cl-、Fe3+、K+ | B. | Cl-、Ag+、NO3-、Na+ | ||
| C. | SO42-、Al3+、Na+、Cl- | D. | NO3-、HCO3-、Na+、SO42- |
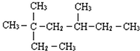 3,3,5-三甲基庚烷
3,3,5-三甲基庚烷 2,3-二甲基-1-丁烯
2,3-二甲基-1-丁烯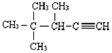 的系统名称为3,4,4-三甲基-1-戊炔.
的系统名称为3,4,4-三甲基-1-戊炔.