题目内容
表示下列变化的化学用语正确的是( )
| A、氨水显碱性:NH3?H2O?NH4++OH- |
| B、醋酸溶液显酸性:CH3COOH=CH3COO-+H+ |
| C、NaHCO3溶液显碱性:HCO3-+H2O?CO32-+OH- |
| D、FeCl3溶液显酸性:Fe3++3H2O=Fe(OH)3↓+3H+ |
考点:弱电解质在水溶液中的电离平衡,盐类水解的原理
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:A.一水合氨为弱电解质,部分电离;
B.醋酸为弱电解质,部分电离;
C.NaHCO3溶液显碱性,水解生成H2CO3;
D.水解程度较小,没有沉淀生成.
B.醋酸为弱电解质,部分电离;
C.NaHCO3溶液显碱性,水解生成H2CO3;
D.水解程度较小,没有沉淀生成.
解答:
解:A.一水合氨为弱电解质,部分电离,电离方程式为NH3?H2O?NH4++OH-,故A正确;
B.醋酸为弱电解质,部分电离,电离方程式为CH3COOH?CH3COO-+H+,故B错误;
C.NaHCO3溶液显碱性,水解生成H2CO3,离子方程式为HCO3-+H2O?H2CO3+OH-,故C错误;
D.水解程度较小,没有沉淀生成,应为Fe3++3H2O=Fe(OH)3+3H+,故D错误.
故选A.
B.醋酸为弱电解质,部分电离,电离方程式为CH3COOH?CH3COO-+H+,故B错误;
C.NaHCO3溶液显碱性,水解生成H2CO3,离子方程式为HCO3-+H2O?H2CO3+OH-,故C错误;
D.水解程度较小,没有沉淀生成,应为Fe3++3H2O=Fe(OH)3+3H+,故D错误.
故选A.
点评:本题综合考查弱电解质的电离和盐类的水解,为高频考点,侧重于学生的分析能力和基本概念的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
如图中的三种常用金属的开发利用之所以有先后,主要取决于( )

| A、金属的导电性强弱 |
| B、金属在地壳中的含量多少 |
| C、金属的化合价高低 |
| D、金属的活动性大小 |
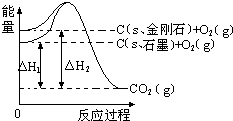 如图所示,△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,下列说法不正确的是( )
如图所示,△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,下列说法不正确的是( )| A、C(s、金刚石)C═(s、石墨)△H=-1.9 kJ?mol-1 |
| B、石墨和金刚石的转化是化学变化 |
| C、1mol金刚石完全燃烧放出的能量比1mol石墨完全燃烧放出的能量多 |
| D、金刚石的稳定性强于石墨 |
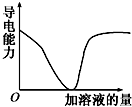 如图所示,纵坐标表示导电能力,横坐标表示所加溶液的量,以下各组反应符合该图的是( )
如图所示,纵坐标表示导电能力,横坐标表示所加溶液的量,以下各组反应符合该图的是( )| A、Ba(OH)2溶液中滴加稀H2SO4 |
| B、NaOH溶液中滴加稀HCl |
| C、CH3COOH溶液中滴加KOH溶液 |
| D、Cu(OH)2悬浊液中滴加HNO3溶液 |
一定条件下,在一密闭容器中将1.0mol/L N2与3.0mol/L H2合成氨,反应到2s时测得NH3的浓度为0.8mol/L,当用氢气浓度的减少来表示该反应的反应速率时,该反应的反应速率为( )
| A、0.2 mol/(L?s) |
| B、0.4 mol/(L?s) |
| C、0.6 mol/(L?s) |
| D、0.8 mol/(L?s) |
下列说法正确的是( )
| A、标准状况下,CO2的气体摩尔体积为22.4L |
| B、标准状况下,4.4g CO2的体积为11.2L |
| C、标准状况下,0.5mol的H2O的体积约为11.2L |
| D、0℃,101kPa时,1molO2和N2的混合气体的总体积约为22.4L |
设NA是阿伏伽德罗常数的数值.下列说法正确的是( )
| A、1L 0.1mol/L的醋酸溶液中,CH3COO-的数目为0.1NA |
| B、标准状况下,8gSO3中含有氧原子的数目为0.3NA |
| C、7.8gNa2O2中含有的阳离子数目为0.1NA |
| D、6mol的二氧化氮和足量的水反应生成硝酸,转移8NA个的电子 |
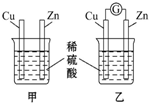 观察如图所示两个实验装置,若两烧杯中硫酸的浓度相同,铜片和锌片都是纯净单质,判断下列叙述正确的是( )
观察如图所示两个实验装置,若两烧杯中硫酸的浓度相同,铜片和锌片都是纯净单质,判断下列叙述正确的是( )| A、两个装置均是原电池装置 |
| B、乙中电子由铜片经过电流计流向锌片 |
| C、过一段时间两烧杯中溶液的酸性均减弱 |
| D、因都是锌与硫酸的反应,所以两装置中产生气泡的速率相同 |
下列有关有机物的说法中正确的是( )
| A、凡是含碳元素的化合物都属于有机物 |
| B、易溶于汽油、酒精、苯等有机溶剂中的物质一定是有机物 |
| C、所有的有机物都很容易燃烧 |
| D、有机物不一定都不溶于水 |