题目内容
下列各组结构和性质对比正确的是( )
| A、第一电离能Li<Na |
| B、电负性O<N |
| C、粒子半径F->Mg2+ |
| D、酸性H2SO3>HNO3 |
考点:元素电离能、电负性的含义及应用
专题:元素周期律与元素周期表专题
分析:A.同一主族元素,第一电离能随着原子序数增大而减小;
B.同一周期元素,元素电负性随着原子序数增大而增大;
C.电子层结构相同的离子,离子半径随着原子序数增大而减小;
D.亚硫酸是弱酸、硝酸是强酸.
B.同一周期元素,元素电负性随着原子序数增大而增大;
C.电子层结构相同的离子,离子半径随着原子序数增大而减小;
D.亚硫酸是弱酸、硝酸是强酸.
解答:
解:A.同一主族元素,第一电离能随着原子序数增大而减小,所以第一电离能Li>Na,故A错误;
B.同一周期元素,元素电负性随着原子序数增大而增大,所以电负性O>N,故B错误;
C.电子层结构相同的离子,离子半径随着原子序数增大而减小,所以离子半径F->Mg2+,故C正确;
D.亚硫酸是弱酸,硝酸是强酸,所以酸性H2SO3<HNO3,故D错误;
故选C.
B.同一周期元素,元素电负性随着原子序数增大而增大,所以电负性O>N,故B错误;
C.电子层结构相同的离子,离子半径随着原子序数增大而减小,所以离子半径F->Mg2+,故C正确;
D.亚硫酸是弱酸,硝酸是强酸,所以酸性H2SO3<HNO3,故D错误;
故选C.
点评:本题考查元素周期律的综合应用,涉及电离能、电负性、离子半径、酸的强弱判断等知识点,侧重考查学生对元素周期律的灵活运用,注意第一电离能规律中的异常现象,知道其成因,题目难度不大.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
2012年2月,国务院同意发布新修订的《环境空气质量标准》增加了PM2.5监测指标,PM2.5是用来监测空气中下列哪项含量的( )
| A、二氧化碳 | B、一氧化碳 |
| C、二氧化硫 | D、可吸入颗粒物 |
化学已经渗透到人类生活的各个方面,下列说法不正确的是( )
| A、食盐可作氯碱工业的原料 |
| B、碘酒是指单质碘的乙醇溶液 |
| C、大量使用化肥和农药,以提高农作物产量,符合绿色化学的原则 |
| D、低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,减少温室气体的排放 |
2mol A与2mol B混合于2L的密闭容器中,发生如下反应:2A(g)+3B(g)?2C(g)+zD(g),若2s后,A的转化率为50%,测得v(D)=0.25mol?L-1?s-1,下列推断正确的是( )
| A、v(B)=0.75 mol?L-1?s-1 |
| B、z=2 |
| C、B的转化率为25% |
| D、C的体积分数约为28.6% |
可用于区别溴蒸气和NO2气体的试剂是( )
| A、淀粉碘化钾溶液 |
| B、FeCl2溶液 |
| C、AgNO3溶液 |
| D、NaOH溶液 |
化学与科学、生产、生活、社会密切相关,下列说法不正确的是( )
| A、PM2.5是指大气中直径小于或等于2.5微米的颗粒物,PM2.5比胶体粒子小,因其比表面积大,故可吸附重金属离子,入肺后对人体产生很大的危害 |
| B、硫酸工业中,从吸收塔上部导出的气体再次通入接触室进行二次氧化,进一步吸收后,二氧化硫的含量很少,可直接排放到空气中 |
| C、以NO和NO2为主的氮氧化物是形成光化学烟雾和酸雨的一个重要原因 |
| D、高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
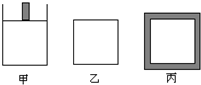 800K时下列起始体积相同的密闭容器中充入2mol SO2、1mol O2,其反应是2SO2(g)+O2(g)?2SO3(g);△H=-96.56kJ?mol-1,△S=-0.19kJ?mol-1?K-1.甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙容器维持绝热,三容器各自建立化学平衡.已知:△H-T?△S<0时,反应能自发进行.
800K时下列起始体积相同的密闭容器中充入2mol SO2、1mol O2,其反应是2SO2(g)+O2(g)?2SO3(g);△H=-96.56kJ?mol-1,△S=-0.19kJ?mol-1?K-1.甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙容器维持绝热,三容器各自建立化学平衡.已知:△H-T?△S<0时,反应能自发进行. 如图是测定镁粉(含铝粉)的纯度的实验装置.所用的NaOH浓度为4.6mol?L-1.
如图是测定镁粉(含铝粉)的纯度的实验装置.所用的NaOH浓度为4.6mol?L-1.