题目内容
 把镁条投入到盛有盐酸的敞口容器里,产生H2的速率如图所示,在下列因素中,影响O~t1时间段反应速率的主要因素是( )
把镁条投入到盛有盐酸的敞口容器里,产生H2的速率如图所示,在下列因素中,影响O~t1时间段反应速率的主要因素是( )| A、盐酸的浓度 |
| B、镁条的表面积 |
| C、Cl-的浓度 |
| D、溶液的温度 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:由图可知,开始反应速率加快,与温度有关,后来反应速率减小与氢离子浓度有关,以此来解答.
解答:
解:镁条投入到盛有盐酸的敞口容器里,发生Mg与盐酸的反应,O~t1时刻,浓度不断减小,反应速率应减小,但放热反应,温度升高,且总体反应速率呈不断增大趋势,说明影响O~t1时间段反应速率的主要因素是温度.
故选D.
故选D.
点评:本题考查影响化学反应速率的因素,为高频考点,把握温度、浓度对反应速率的影响为解答的关键,侧重分析与知识应用能力的考查,注意反应为放热反应,题目难度不大.

练习册系列答案
相关题目
现有200mLNH4HCO3和Na2CO3的混合溶液,加入含a mol氢氧化钠的溶液并加热,恰好反应完全;继续加入含bmolHCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为( )
| A、(0.5b-0.5a)mol/L | ||
| B、(2b-a)mol/L | ||
C、(5b-
| ||
| D、(5b-5a)mol/L |
设NA为阿伏加德罗常数的数值.下列说法正确的是( )
| A、常温常压下,8gO2含有4NA个电子 |
| B、l L 0.1 mol?L-1的氨水中含有0. 1NA个NH+4 |
| C、标准状况下,22.4 L盐酸含有NA个lHC1分子 |
| D、1 mol Na被完全氧化生成Na2O2,失去2NA个电子 |
下列各组互为等电子体的是( )
| A、N2O和NO2 |
| B、O3和SO2 |
| C、CH4和NH3 |
| D、OH-和NH2- |
下列各组中的性质比较中,不正确的是( )
| A、酸性 HClO4>HBrO4>HIO4 |
| B、碱性 Ba(OH)2>Ca(OH)2>Mg(OH)2 |
| C、还原性 F->Cl->Br- |
| D、稳定性 HCl>H2S>PH3 |
水的电离平衡曲线如图所示,下列说法不正确的是( )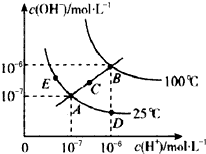

| A、图中五点KW间的关系:B>C>A=D=E |
| B、若从A点到D点,可采用:温度不变在水中加入少量的酸 |
| C、若处在B点时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性 |
| D、若从A点到C点,可采用:温度不变在水中加入适量的NH4Cl固体 |
在一定温度下,将X和Y 各0.16mol充入10L 恒容密闭容器中,发生反应:2X(g)+Y(s)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表下列说法正确的是( )
| t/s | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.10 | 0.09 | 0.09 |
| A、反应前2s的平均速率v(Z)=2.0×10-3 mol/(L?s) |
| B、其他条件不变,加入一定量的Y,反应速率一定加快 |
| C、反应进行4s时,X的转化率75% |
| D、反应达到平衡时,X的物质的量浓度为0.02mol?L-1 |
用同一种烧碱溶液分别中和物质的量浓度和体积都相同的盐酸、硫酸、硝酸,恰好反应完全时,消耗烧碱溶液的体积分别为aL、bL、cL,则a、b、c的数值关系是( )
| A、a=b=c | ||
B、a=
| ||
| C、a=2b=c | ||
| D、a≠b≠c |
 常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如图所示.
常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如图所示.