题目内容
8.某有机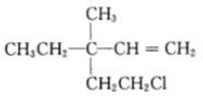 具有手性碳原子,经下面的变化后仍一定具有手性碳原子的是( )
具有手性碳原子,经下面的变化后仍一定具有手性碳原子的是( )| A. | 加成反应 | B. | 消去反应 | C. | 氯代反应 | D. | 水解反应 |
分析 由结构可知,不含H原子的C上连接4个不同基团,为手性碳原子,分子中含碳碳双键、-Cl,结合烯烃、卤代烃的性质来解答.
解答 解:A.碳碳双键与氢气发生加成反应,中间C连接2个-CH2CH3,不具有手性,故A不选;
B.-Cl发生消去反应后,中间C连接2个-CH=CH2,不具有手性,故B不选;
C.若最左侧的甲基发生氯代反应,中间C连接2个-CH2CH2Cl,不具有手性,故C不选;
D.-CH2CH2Cl发生水解反应转化为-CH2CH2OH,中间C上连接4个不同基团,为手性碳原子,故D选;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意烯烃、卤代烃的性质,题目难度不大.

练习册系列答案
 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
19.如表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是( )
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.071 | 0.099 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -1 |
| A. | A、B简单离子半径大小关系为B3+>A2+ | |
| B. | A、B、E对应原子的第一电离能大小为:E>A>B | |
| C. | 气态氢化物的稳定性:HD<H2C | |
| D. | 最高价氧化物对应的水化物的酸性:H2CO4>HEO4 |
16.白藜芦醇 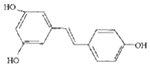 ,广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性.能够跟1mol该化合物起反应的Br2或H2的最大用量分别是( )
,广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性.能够跟1mol该化合物起反应的Br2或H2的最大用量分别是( )
 ,广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性.能够跟1mol该化合物起反应的Br2或H2的最大用量分别是( )
,广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性.能够跟1mol该化合物起反应的Br2或H2的最大用量分别是( )| A. | 1mol,1mol | B. | 3.5mol,7mol | C. | 3.5mol,6mol | D. | 6mol,7mol |
3.X、Y、Z、W是原子序数依次增大的短周期元素,它们的最外层电子数分别为1、1、6、7.X-的电子层结构与氦相同,Y、Z和W的次外层有8个电子.下列叙述错误的是( )
| A. | 元素X、Z、W各自最高和最低化合价的代数和分别为1、4、6 | |
| B. | 原子半径的大小为Y>Z>W | |
| C. | 元素的非金属性顺序为W>Z>X | |
| D. | Y和其他3种元素均能形成离子化合物 |
13.在恒温恒容密闭容器中发生反应NH2COONH4(s)?2NH3(g)+CO2(g),不能判断该反应已达到化学平衡的是( )
| A. | 2v(NH3)=v(CO2) | |
| B. | 密闭容器中总压强不变 | |
| C. | 密闭容器中混合气体的密度不变 | |
| D. | 密闭容器中混合气体的平均摩尔质量不变 |
20.A和B均为短周期元素,它们的离子A-和B2+具有相同的核外电子层结构.下面说法正确的是( )
| A. | 原子序数A>B | B. | 核外电子数为B>A | C. | 原子半径A>B | D. | 离子半径 B2+>A- |
13.已知:pOH=-lgc(OH-),298K时,向20.00mL0.10mol•L-1氨水中滴入0.10mol•L-1的盐酸,溶液的pH和pOH与加入盐酸体积关系如图所示.下列说法正确的是( )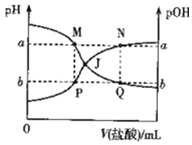

| A. | 曲线PJN表示溶液中pH的变化 | |
| B. | M点水的电离程度比Q点大 | |
| C. | M、P两点的数值之和a+b=14 | |
| D. | pH与pOH交叉点J对应的V(盐酸)=20.00 mL |
 $\stackrel{铑催化剂}{→}$
$\stackrel{铑催化剂}{→}$ (R1代表氢原子或烃基)
(R1代表氢原子或烃基)
 +
+ $\stackrel{碱}{→}$
$\stackrel{碱}{→}$ +H2O
+H2O .
. .
.