题目内容
12.关于下列装置说法正确的是( )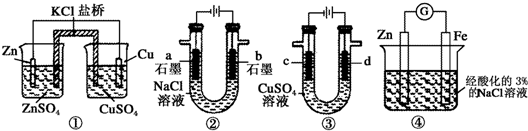
| A. | 装置①中,一段时间后左侧SO42-浓度增大 | |
| B. | 装置②中滴入酚酞,b极附近先变红 | |
| C. | 用装置③精炼铜时,c极为粗铜 | |
| D. | 装置④中在Fe电极附近滴入K3[Fe(CN)6]溶液,可验证Fe电极被保护 |
分析 A.装置①是原电池,溶液中SO42-不参加反应;
B.电解时,b是阳极、a是阴极,阳极上生成氯气、阴极上生成氢气,且阴极附近有NaOH生成,溶液呈碱性;
C.电解精炼粗铜时,粗铜作阳极、纯铜作阴极;
D.原电池中Zn为负极,保护了铁.
解答 解:A.装置①是原电池,溶液中SO42-不参加反应,所以放电过程中硫酸根离子浓度不变,故A错误;
B.电解时,b是阳极、a是阴极,阳极上生成氯气、阴极上生成氢气,且阴极附近有NaOH生成,溶液呈碱性,所以a电极附近溶液呈红色,故B错误;
C.电解精炼粗铜时,粗铜作阳极、纯铜作阴极,所以d为粗铜,故C错误;
D.原电池中Zn为负极,Fe不会失去电子,Fe电极附近滴入K3[Fe(CN)6]溶液无现象可验证Fe电极被保护,故D正确;
故选D.
点评 本题以原电池和电解池为载体考查化学实验方案评价,为高频考点,明确实验原理是解本题关键,知道各个电极上发生的反应,比较容易.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
2.植物及其废弃物可以制取乙醇燃料,下列关于乙醇燃料的说法错误的是( )
| A. | 它与甲醚(CH3-O-CH3)互为同分异构体 | |
| B. | 乙醇易燃烧,污染小 | |
| C. | 乙醇只能在实验室内作燃料 | |
| D. | 粮食作物是制乙醇的重要原料 |
7.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 在标准状况下,44.8L CH2Cl2所含有的分子数为2NA | |
| B. | 42 g乙烯和丙烯(C3H6)的混合气体中含有的碳原子数为3NA | |
| C. | 100 mL 0.1 mol/L的FeCl3溶液中含有Fe3+的个数为0.01 NA | |
| D. | 粗铜精炼时转移1mol电子,阳极上溶解的Cu原子数一定为0.5 NA |
2.1985年,科学家发现一种新的分子组成的物质,其化学式为60,下列有关的说法不正确的是( )
| A. | 它的式量为720 | |
| B. | 它是一种单质 | |
| C. | 它是一种新型的共价化合物 | |
| D. | 它在氧气中燃烧的产物和碳在氧气中燃烧的产物相同 |

 .
.
 +4NaOH$\stackrel{△}{→}$2CH3COONa+
+4NaOH$\stackrel{△}{→}$2CH3COONa+ +4H2O.
+4H2O.


 的同分异构体中同时符合下列条件的芳香族化合物共有6种.
的同分异构体中同时符合下列条件的芳香族化合物共有6种. (任写一种)(任写一种).
(任写一种)(任写一种). ,CH(CH3)3的名称为:2-甲基丙烷.
,CH(CH3)3的名称为:2-甲基丙烷.