题目内容
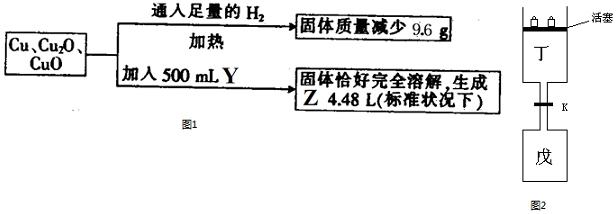
9. “霾”是当今世界环境热点话题.某地空气质量恶化原因之一是机动车尾气和燃煤产生的烟气.NO和CO气体均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:
“霾”是当今世界环境热点话题.某地空气质量恶化原因之一是机动车尾气和燃煤产生的烟气.NO和CO气体均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:2NO(g)+2CO(g)$\stackrel{催化剂}{?}$2CO2(g)+N2(g)△H=-akJ•mol-1(a>0)
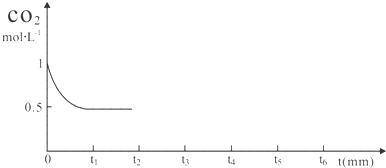
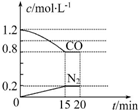
(1)在一定温度下,将2.0mol NO、2.4mol CO气体通入固定容积为2L的密闭容器中,反应过程中部分物质的浓度变化如图所示:
①0~15min N2的平均速率v(N2)=0.013mol/(L•min);NO的转化率为40%.
②20min时,若改变反应条件,导致CO浓度减小,则改变的条件可能是cd(选填序号).
a.缩小容器体积
b.增加CO的量
c.降低温度
d.扩大容器体积
③若保持反应体系的温度不变,20min时再向容器中充入NO、N2各0.4mol,化学平衡将向左移动(选填“向左”“向右”或“不”),重新达到平衡后,该反应的化学平衡常数为$\frac{5}{36}$.
(2)已知:2NO(g)+O2(g)═2NO2(g)△H=-bkJ•mol-1(b>0)
CO的燃烧热△H=-ckJ•mol-1(c>0)
则在消除汽车尾气中NO2的污染时,NO2与CO发生反应的热化学方程式为4CO(g)+2NO2(g)?N2(g)+4CO2(g)△H=(-a+b-2c) kJ•mol-1.
分析 (1)①根据v=$\frac{△c}{△t}$计算v(N2);利用浓度变化量之比等于化学计量数之比计算NO浓度变化量,再根据n=cV计算参加反应NO的物质的量,进而计算NO的转化率;
②a.缩小容器体积,压强增大,平衡向正反应方向移动,移动结果不能消除CO浓度增大;
b.增加CO的量,CO的浓度增大;
c.降低温度,平衡向正反应方向移动;
d.扩大容器体积,压强减小,平衡向逆反应方向移动,平衡时CO浓度减小;
③温度不变,平衡常数不变,利用三段式计算平衡时各组分的浓度,代入平衡常数K=$\frac{{c}^{2}(C{O}_{2})•c({N}_{2})}{c(NO)•{c}^{2}(CO)}$,再计算此时浓度商Qc,与平衡常数相比,判断反应进行方向;
(2)根据CO的燃烧热书写CO燃烧的热化学方程式,根据盖斯定律,由已知热化学方程式乘以合适的系数进行加减构造目标热化学方程式,反应热也进行相应的计算.
解答 解:(1)①由图可知,15min N2的浓度变化量为0.2mol/L,则v(N2)=$\frac{0.2mol/L}{15min}$=0.013mol/(L•min);
浓度变化量之比等于化学计量数之比,则NO浓度变化量为2×0.2mol/L=0.4mol/L,参加反应的NO为2L×0.4mol/L=0.8mol,所以NO的转化率为:$\frac{0.8mol}{2mol}$×100%=40%,
故答案为:0.013mol/(L•min);40%;
②a.缩小容器体积,压强增大,平衡向正反应方向移动,移动结果不能消除CO浓度增大,平衡时CO浓度增大,故a错误;
b.增加CO的量,平衡虽然向正反应方向移动,但CO的转化率减小,到平衡时CO的浓度增大,故b错误;
c.降低温度,平衡向正反应方向移动,到达新平衡时CO的浓度减小,故c正确;
d.扩大容器体积,压强减小,平衡向逆反应方向移动,但CO的物质的量增大程度小于体积增大程度,所以CO浓度减小,故d正确;
故答案为:cd;
③平衡时氮气浓度变化量为0.2mol/L,NO的起始浓度为:$\frac{2mol}{2L}$=1mol/L、CO的起始浓度为 $\frac{2.4mol}{2L}$=1.2mol/L,则:
2NO(g)+2CO(g)?2CO2(g)+N2(g)
开始(mol/L):1 1.2 0 0
转化(mol/L):0.4 0.4 0.4 0.2
平衡(mol/L):0.6 0.8 0.4 0.2
故平衡常数为:K=$\frac{{c}^{2}(C{O}_{2})•c({N}_{2})}{{c}^{2}(NO)•{c}^{2}(CO)}$=$\frac{0.{4}^{2}×0.2}{0.{6}^{2}×0.{8}^{2}}$L/mol=$\frac{5}{36}$L/mol,
20min时再向容器中充入NO、N2各0.4mol,此时浓度商Qc=$\frac{0.{4}^{2}×(0.2+\frac{0.4}{2})}{(0.6+\frac{0.4}{2})^{2}×0.{8}^{2}}$=$\frac{5}{32}$>K=$\frac{5}{36}$,故反应向逆反应进行,即向左移动,
温度不变,平衡常数不变,即重新达到平衡后,该反应的化学平衡常数为$\frac{5}{36}$,
故答案为:向左;$\frac{5}{36}$;
(2))①2CO(g)+2NO(g)?N2(g)+2CO2(g)△H=-a kJ•mol-1
②2NO(g)+O2(g)=2NO2(g)△H=-b kJ•mol-1
③CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-c kJ•mol-1
根据盖斯定律,①-②+2×③得:4CO(g)+2NO2(g)?N2(g)+4CO2(g)△H=(-a+b-2c )kJ•mol-1,
故答案为:4CO(g)+2NO2(g)?N2(g)+4CO2(g)△H=(-a+b-2c) kJ•mol-1.
点评 本题考查较为综合,涉及化学平衡有关计算、化学平衡移动、化学反应速率计算、平衡常数计算及应用、热化学方程式书写等知识,题目难度中等,化学平衡常数的有关计算是高考热点,理解掌握化学平衡常数与浓度商的关系确定反应方向,(1)②为易错点,学生容易根据平衡移动判断浓度变化,注意对平衡移动原理的理解:“减弱改变”而不是“消除改变”,也可以借助平衡常数理解.

| A. | 加入硫酸铜可使锌与稀硫酸的反应速率加快,说明Cu2+具有催化作用 | |
| B. | 向某溶液中滴加硝酸酸化的BaCl2溶液产生白色沉淀,则该溶液中含有SO42- | |
| C. | 在电解精炼铜过程中,阳极质量的减少多于阴极质量的增加 | |
| D. | 298 K时,2H2S(g)+SO2(g)=3S(s)+2H2O(l)能自发进行,则其△H<0 |
| A. | H2O与D2O互为同位素 | B. | 纤维素与淀粉互为同分异构体 | ||
| C. | 干冰和冰为同一种物质 | D. | 甲烷和十六烷互为同系物 |
反应②Fe(s)+H2O(g)═FeO(s)+H 2 (g) 平衡常数为 K2;
测得在不同温度下,K1、K2值如下:
| 温度/℃ | K1 | K2 |
| 500 | 1.00 | 3.15 |
| 700 | 1.47 | 2.26 |
| 900 | 2.40 | 1.60 |
(2)在 900℃时反应 CO2(g)+H2(g)═CO(g)+H2O(g)的平衡常数 K=1.50.
(3)700℃反应②达到平衡,其它条件不变时,使得该平衡向右移动,可以采取的措施有BC(选填编号).
A.缩小反应器体积 B.加入水蒸气
C.降低温度到500℃D.加入Fe粉
(4)如果上述反应①在体积不变的密闭容器中发生,能说明反应已达到平衡状态的是AC(选填编号).
A.v正(CO)=v 逆 (CO2) B.C(CO)=C(CO2)
C.容器内气体的密度不变 D.容器内压强不变
(5)若反应①在体积固定的密闭容器中进行,在一定条件下达到平衡状态,改变下列条件再达平衡后,相应物质的物理量如何变化?(选填“增大”、“减小”或“不变”)
①降低温度,CO2的平衡浓度增大;
②再通入CO2,CO2的转化率不变.
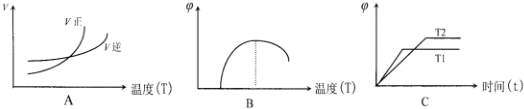
(6)下列图象符合反应①的是A(填序号)(图中 v 是速率、φ 为混合其中CO含量,T为温度)
| 选项 | 实验事实 | 结论 |
| A | 其他条件相同,Na2S2O3溶液浓度越大,与同浓度的硫酸反应析出流沉淀所需的时间越短 | 当其他条件不变时,增大反应物浓度,化学反应速率增大 |
| B | 用铜作电极电解CuSO4溶液,CuSO4溶液浓度不变 | Cu2+没有参与电极反应 |
| C | 在常温下N2不能与O2反应,而白磷却能自燃 | 氮元素的非金属性比磷元素的弱 |
| D | 醋酸能与碱反应 | 醋酸分子一定不能存在于碱性溶液中 |
| A. | A | B. | B | C. | C | D. | D |