题目内容
阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是( )
| A、标准状况下,33.6L H2O含有9.03×1023个H2O分子 |
| B、0.1L 3mol?L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023 |
| C、5.6g铁粉与硝酸反应失去的电子数一定为0.3×6.02×1023 |
| D、1mol Cl2与足量Fe反应,转移的电子数为2×6.02×1023 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
B.硝酸铵溶液中,铵根离子部分水解,溶液中铵根离子数目减少;
C.铁为变价金属,反应产物中铁元素的化合价可能为+2或+3价,如果硝酸不足,0.1mol铁完全反应最多失去0.2mol电子;
D.1mol氯气与铁完全反应最多得到2mol电子.
B.硝酸铵溶液中,铵根离子部分水解,溶液中铵根离子数目减少;
C.铁为变价金属,反应产物中铁元素的化合价可能为+2或+3价,如果硝酸不足,0.1mol铁完全反应最多失去0.2mol电子;
D.1mol氯气与铁完全反应最多得到2mol电子.
解答:
解:A.标况下,水不是气体,不能使用标况下的气体摩尔体积金属33.6L水的物质的量,故A错误;
B.0.1L 3mol?L-1的NH4NO3溶液中含有溶质硝酸铵0.3mol,由于铵根离子部分水解,则溶液中含有的铵根离子的数目小于0.3×6.02×1023,故B错误;
C.5.6g铁的物质的量为0.1mol,0.1mol铁与硝酸反应可能生成0.1mol亚铁离子,失去的电子为0.2mol,则转移的电子数目为0.2×6.02×1023,故C错误;
D.1mol氯气与铁反应生成氯化铁,最多得到2mol电子,转移的电子数为2×6.02×1023,故D正确;
故选D.
B.0.1L 3mol?L-1的NH4NO3溶液中含有溶质硝酸铵0.3mol,由于铵根离子部分水解,则溶液中含有的铵根离子的数目小于0.3×6.02×1023,故B错误;
C.5.6g铁的物质的量为0.1mol,0.1mol铁与硝酸反应可能生成0.1mol亚铁离子,失去的电子为0.2mol,则转移的电子数目为0.2×6.02×1023,故C错误;
D.1mol氯气与铁反应生成氯化铁,最多得到2mol电子,转移的电子数为2×6.02×1023,故D正确;
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下水的状态不是气体,试题有利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
下列物质属于纯净物的是( )
| A、漂白粉 | B、液氨 | C、氯气 | D、盐酸 |
下列关于胶体的有关说法中,不正确的是( )
| A、用丁达尔效应可以鉴别氯化铁溶液和氢氧化铁胶体 |
| B、胶体在一定条件下能稳定存在,属于介稳体系 |
| C、少数胶体属于纯净物 |
| D、胶体、溶液和浊液的本质区别是分散质粒子的大小不同 |
据最新报道,科学家发现了如下反应;O2+PtF6═O2[PtF6],已知O2[PtF6]为配位化合物(其中Pt为+5价,O显正价,且是科学家最新发现的显正价的氧元素),对此反应,下列说法正确的是( )
| A、该配合物的配位原子是F和O,配位数为8 |
| B、在此反应中,O2是氧化剂,PtF6是还原剂 |
| C、O2[PtF6]中Pt与F之间以离子键相结合 |
| D、反应中每生成1mol O2(PtF6),转移1mol电子 |
下列表述错误的是( )
| A、氨具有还原性,可用于制硝酸 |
| B、Cl2可用于制漂白粉和农药生产 |
| C、利用浓硫酸的脱水性,可干燥Cl2、SO2气体 |
| D、NaHCO3治疗胃酸过多的一种药剂 |
下列烷烃在光照下与氯气反应,只生成一种一氯代烃的是( )
| A、CH3CH2CH3 |
B、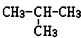 |
C、 |
D、 |
下列属于取代反应的是( )
A、H2C=CH2+H2
| ||
B、2CH3CH2OH+O2
| ||
C、 +3H2 +3H2
 | ||
D、 +3NaOH +3NaOH
 |
在下列各说法中,正确的是( )
| A、反应MgCl2(l)=Mg(l)+Cl2(g)的△H<0,△S>0 |
| B、熵是一个与内能有关的物理量 |
| C、1mol H2SO4与1mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热 |
| D、1mol H2与0.5mol O2反应放出的热就是H2的燃烧热 |