题目内容
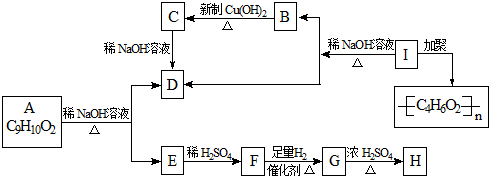
根据下面的反应线路及所给信息填空.
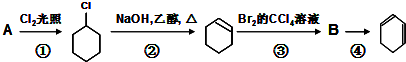
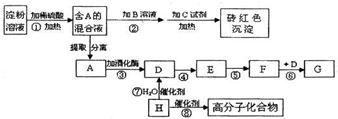
(1)B的结构简式是 ;
(2)④的反应类型是 ;
(3)写出反应②的化学方程式 .

(1)B的结构简式是
(2)④的反应类型是
(3)写出反应②的化学方程式
考点:有机物的推断
专题:有机物的化学性质及推断
分析:由反应①可知A为环己烷,反应②发生消去反应,反应③环己烯与溴发生加成反应生成B为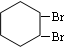 ,B在氢氧化钠醇溶液、加热条件下发生消去反应生成
,B在氢氧化钠醇溶液、加热条件下发生消去反应生成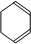 ,据此解答.
,据此解答.
 ,B在氢氧化钠醇溶液、加热条件下发生消去反应生成
,B在氢氧化钠醇溶液、加热条件下发生消去反应生成 ,据此解答.
,据此解答.解答:
解:由反应①可知A为环己烷,反应②发生消去反应,反应③环己烯与溴发生加成反应生成B为 ,B在氢氧化钠醇溶液、加热条件下发生消去反应生成
,B在氢氧化钠醇溶液、加热条件下发生消去反应生成 ,据此
,据此
(1)由上述分析可知,B的结构简式是 ,故答案为:
,故答案为: ;
;
(2)反应④是 发生消去反应生成
发生消去反应生成 ,故答案为:消去反应;
,故答案为:消去反应;
(3)反应②是卤代烃发生消去反应生成烯烃,反应化学方程式为: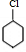 +NaOH
+NaOH
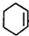 +NaCl+H2O,故答案为:
+NaCl+H2O,故答案为: +NaOH
+NaOH
 +NaCl+H2O.
+NaCl+H2O.
 ,B在氢氧化钠醇溶液、加热条件下发生消去反应生成
,B在氢氧化钠醇溶液、加热条件下发生消去反应生成 ,据此
,据此(1)由上述分析可知,B的结构简式是
 ,故答案为:
,故答案为: ;
;(2)反应④是
 发生消去反应生成
发生消去反应生成 ,故答案为:消去反应;
,故答案为:消去反应;(3)反应②是卤代烃发生消去反应生成烯烃,反应化学方程式为:
 +NaOH
+NaOH| 醇 |
| △ |
 +NaCl+H2O,故答案为:
+NaCl+H2O,故答案为: +NaOH
+NaOH| 醇 |
| △ |
 +NaCl+H2O.
+NaCl+H2O.
点评:本题考查有机物推断、有机反应类型、有机方程式书写,难度不大,注意根据有机物的结构判断发生的反应,关键是掌握官能团的性质与转化.

练习册系列答案
 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案
相关题目
A、B、C、D、E均含有同一种短周期元素,其中A是单质,B常温下是气态氢化物,C、D是氧化物,E是D和水反应的产物.下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是:( )
| 物质 编号 | 物质转化关系 | A | D | E |
| ① | 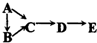 | Si | SiO2 | H2SiO3 |
| ② | N | NO2 | HNO3 | |
| ③ | S | SO2 | H2SO4 | |
| ④ | Na | Na2O2 | NaOH |
| A、①②③④ | B、②③ |
| C、①③④ | D、②④ |
已知:
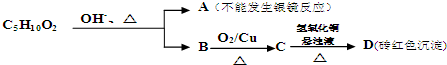
则符合要求的C5H10O2的结构有( )
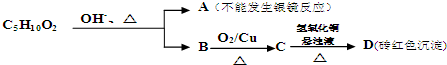
则符合要求的C5H10O2的结构有( )
| A、1种 | B、2种 | C、4种 | D、5种 |
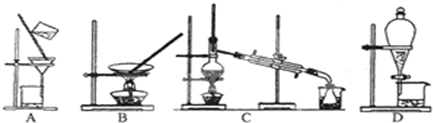
下列实验操作正确的是( )
A、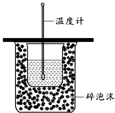 用如图装置测定中和热 |
| B、中和滴定过程中,眼睛应注视锥形瓶内溶液颜色的变化 |
| C、研究H+浓度对该平衡:Cr2O72-+H2O?2CrO42-+2H+的影响,往5mL 0.1mol/L K2CrO4溶液加入5mL 0.1mol/L的稀硫酸 |
| D、测定溶液的pH值时,用玻璃棒蘸取少量溶液点在湿润的pH试纸上再与标准比色卡对照 |
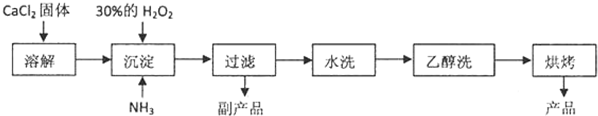
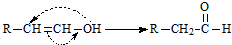 化学式为C9H10O2的有机物A有如下的转化关系
化学式为C9H10O2的有机物A有如下的转化关系