题目内容
20.现有X、Y、Z、W四种短周期元素.①X元素的单质在Y元素的单质中燃烧发出苍白色火焰,并生成气体A.
②Z元素的单质与A的水溶液反应又生成X元素的单质.
③Z元素的原子和Y元素的原子电子层数相同,且它们的最外层电子数之差的绝对值为奇数.
④W元素的原子核外有3个电子层,其最外层电子数等于电子层数.
请回答下列问题:
(1)X的元素符号为:H;Z的元素名称是:镁.
(2)A的电子式是
 .
.(3)Z的单质与A的溶液反应的离子方程式Mg+2H++=Mg2++H2↑.
(4)W的氧化物溶于NaOH中的化学方程式Al2O3+2OH-=2AlO2-+H2O.
分析 ①X元素的单质在Y元素的单质中燃烧发出苍白色火焰,并生成气体A,则X为H元素,Y为Cl元素,A为HCl;
②Z元素的单质与HCl溶液反应生成氢气,则Z为金属元素;
③Z元素的原子和Cl元素的原子电子层数相同,且它们的最外层电子数之差的绝对值为奇数,则Z的最外层有2个电子,所以Z为Mg元素;
④W元素的原子核外有3个电子层,其最外层电子数等于电子层数,则最外层电子数为3,所以W为Al元素;
结合元素化合物的性质及元素周期律解答.
解答 解:①X元素的单质在Y元素的单质中燃烧发出苍白色火焰,并生成气体A,则X为H元素,Y为Cl元素,A为HCl;
②Z元素的单质与HCl溶液反应生成氢气,则Z为金属元素;
③Z元素的原子和Cl元素的原子电子层数相同,且它们的最外层电子数之差的绝对值为奇数,则Z的最外层有2个电子,所以Z为Mg元素;
④W元素的原子核外有3个电子层,其最外层电子数等于电子层数,则最外层电子数为3,所以W为Al元素;
(1)X的元素符号为:H;Z的元素名称是:镁;
故答案为:H;镁;
(2)A为HCl,HCl分子是由1个氢原子和1个氯原子通过共用1对电子结合而成的共价化合物其电子式为 ,
,
故答案为: ;
;
(3)Mg与HCl溶液反应生成氯化镁和氢气,其反应的离子方程式为:Mg+2H++=Mg2++H2↑,故答案为:Mg+2H++=Mg2++H2↑;
(4)W为Al元素,其氧化物为两性氧化物,能与NaOH反应,其反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O,故答案为:Al2O3+2OH-=2AlO2-+H2O.
点评 本题考查了元素的推断和元素周期律的应用,注意把握元素单质及化合物的转化关系、常用化学用语书写等,题目难度不大,注意基础知识的掌握.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
10.下列说法正确的是( )
| A. | KOH和CaCl2既含有离子键,又含有共价键 | |
| B. | PH3各原子均满足8电子稳定结构 | |
| C. | 硫离子的结构示意图: | |
| D. | NH4Cl的电子式: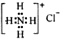 |
11.下列化学用语正确的是( )
| A. | HCl的电子式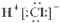 | B. | Cl-的结构示意图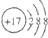 | ||
| C. | CO2的电子式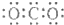 | D. | 质量数为37的氯原子37Cl |
8.短周期元素Q、W、X、Y、Z在元素周期表中的对应位置如图所示,其中只有Z为金属元素.下列说法正确的是( )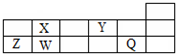

| A. | W、X两元素在自然界中都存在相应的单质 | |
| B. | Q、Y分别与钠元素形成的化合物中仅含离子键 | |
| C. | 简单离子半径由大到小的顺序为:Q>Y>Z | |
| D. | X、Z的最高价氧化物对应的水化物之间易发生化学反应 |
9. 某学生利用物质间的互变,设计成一个平面魔方,如图所示:
某学生利用物质间的互变,设计成一个平面魔方,如图所示:
已知:
①A、B、C、D、G含有同种元素.
②E 是通常情况下密度最小的气体;B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀.B具有氧化性,液显黄色,能将SO2氧化为F(H2SO4),F与A反应生成E、G.
③
依据以上信息填空:
(1)请写出E的电子式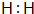 .
.
(2)D的化学式Fe2O3.
(3)请写出ABCDG所含的同种元素的原子结构示意图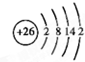 .
.
(4)G生成C的过程中所出现的现象为先产生白色沉淀,逐渐变为灰绿色,最后变为红褐色
(5)写出A→B化学方程式:2Fe+3Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3
(6)B→F的离子方程式为2Fe3++SO2+2H2O═2Fe2++SO42-+4H+.
 某学生利用物质间的互变,设计成一个平面魔方,如图所示:
某学生利用物质间的互变,设计成一个平面魔方,如图所示:已知:
①A、B、C、D、G含有同种元素.
②E 是通常情况下密度最小的气体;B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀.B具有氧化性,液显黄色,能将SO2氧化为F(H2SO4),F与A反应生成E、G.
③
| 纯A(单质) | B溶液 | C固体 | D固体 | G溶液 |
| 颜色 | 银白色(粉末状时为黑色)黄色红 | 褐色 | 红棕色 | 浅绿色 |
(1)请写出E的电子式
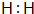 .
.(2)D的化学式Fe2O3.
(3)请写出ABCDG所含的同种元素的原子结构示意图
 .
.(4)G生成C的过程中所出现的现象为先产生白色沉淀,逐渐变为灰绿色,最后变为红褐色
(5)写出A→B化学方程式:2Fe+3Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3
(6)B→F的离子方程式为2Fe3++SO2+2H2O═2Fe2++SO42-+4H+.
10.下列有机物命名正确的是( )
| A. | 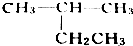 2-乙基丙烷 2-乙基丙烷 | B. | CH3CH2C≡CH 1-丁炔 | ||
| C. | 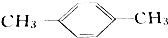 间二甲苯 间二甲苯 | D. | 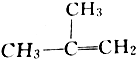 2-甲基-2-丙烯 2-甲基-2-丙烯 |
 工业上合成甲醇的反应为:CO(g)+2H2(g)?CH3OH(g)△H<0.500℃,5MPa条件下,将0.20mol CO与0.58mol H2的混合气体充入2L恒容密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示
工业上合成甲醇的反应为:CO(g)+2H2(g)?CH3OH(g)△H<0.500℃,5MPa条件下,将0.20mol CO与0.58mol H2的混合气体充入2L恒容密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示 某化学兴趣小组为探究元素性质的递变规律,设计可如下系列实验.
某化学兴趣小组为探究元素性质的递变规律,设计可如下系列实验.