题目内容
3.电解质溶液有许多奇妙之处,下列关于电解质溶液的叙述中正确的是( )| A. | Na2CO3、NaHCO3两种盐溶液中,离子种类不相同 | |
| B. | 物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,c(NH4+)前者小于后者 | |
| C. | 常温下,某溶液中由水电离出的c(H+)=10-5mol•L-1,则此溶液可能是盐酸 | |
| D. | 常温下,1 mol•L-1的CH3COOH溶液与1 mol•L-1的NaOH溶液等体积混合后,所得混合液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
分析 A、CO32-在水溶液中水解分步进行;HCO3-在溶液中既能水解又能电离;
B、从盐类水解的影响因素以及平衡移动的角度分析;
C、盐酸溶液中水的电离被抑制;
D、常温下,1 mol•L-1的CH3COOH溶液与1 mol•L-1的NaOH溶液等体积混合后两者恰好完全反应生成CH3COONa.
解答 解:A、CO32-在水溶液中水解分步进行:CO32-+H2O?HCO3-+OH-;HCO3-+H2O?H2CO3+OH-;HCO3-在溶液中既能水解又能电离:HCO3-+H2O?H2CO3+OH-、HCO3-?CO32-+H+,故两溶液中离子种类相同,故A错误;
B、等物质的量浓度的NH4HSO4与NH4Cl溶液,NH4HSO4电离出的H+对NH4+的水解起到抑制作用,所以c(NH4+):前者>后者,故B正确;
C、盐酸溶液中水的电离被抑制,水电离出的c(H+)<10-7mol•L-1,故当水电离出的c(H+)=10-5mol•L-1时,溶液不可能是酸溶液,故C错误;
D、常温下,1 mol•L-1的CH3COOH溶液与1 mol•L-1的NaOH溶液等体积混合后两者恰好完全反应生成CH3COONa,故溶液显碱性,应有:c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故D错误.
故选B.
点评 本题考查了盐类的水解平衡的移动,明确影响平衡移动的因素即可解答,易错选项是C,注意酸和碱均抑制水的电离,而盐类的水解促进水的电离.

练习册系列答案
相关题目
13.下列各电子式中书写正确的是( )
| A. | 氮气 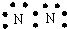 | B. | 氯化氢 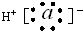 | C. | 氨气 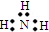 | D. | 氯化镁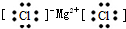 |
14.在汽车排气管加装催化装置,可有效减少CO和NOx的排放,催化装置内发生反应为:NOx+CO$\stackrel{催化剂}{→}$N2+CO2(未配平),下列关于此反应的说法中错误的是( )
| A. | 当x=2时,每生成lmolN2,转移电子数为4mol | |
| B. | 该反应中化合价变化的有N和C元素 | |
| C. | 等物质的量N2和C02中,共用电子对的个数比为3:4 | |
| D. | 氧化剂与还原剂的物质的量之比为1:1时,NOx中氮元素的化合价为+2价 |
18.在蒸发皿中加热蒸干再加热(低400℃)下列物质的溶液,可以得到该物质固体的是( )
| A. | AlCl3 | B. | Na2CO3 | C. | Na2SO3 | D. | MgSO4 |
8.同温同压条件下,在两个容积相同的密闭容器中,一个盛有NH3,另一个盛有N2、H2的混合气体,两容器内的气体一定具有相同的( )
| A. | 原子数 | B. | 分子数 | C. | 质量 | D. | 密度 |
15.以下反应属于氧化还原反应的是( )
| A. | CaO+H2O═Ca(OH)2 | B. | 2NH4HCO3$\stackrel{△}{→}$2NH3↑+H2O+CO2↑ | ||
| C. | 4HCl+O2$\stackrel{△}{→}$2H2O+2Cl2 | D. | NaHCO3+NaHSO4═Na2SO4+CO2↑+H2O |