题目内容
10.将一定量的铁粉加入到装有200mL某浓度的稀硝酸溶液的容器中充分反应.①容器中剩余m1 g铁粉,收集到NO标准状况下体积为672mL.
所得溶液中溶质的化学式Fe(NO3)2,原硝酸溶液的物质的量浓度0.6mol/L.
②向上述固、液混合物中逐滴加入稀硫酸,直到不再产生NO气体为止,此时容器中还剩余铁粉m2g
则此时溶液中溶质的化学式FeSO4,m1-m2 的值为7.6g(精确到0.1g )
分析 (1)①容器中剩有m1 g的铁粉,生成硝酸亚铁;
②硝酸完全反应生成硝酸亚铁与NO,根据n=$\frac{V}{Vm}$计算NO的物质的量,根据电子转移守恒计算参加反应的n(Fe),由氮元素守恒可知:n(HNO3)=2n[Fe(NO3)2]+n(NO),再根据c=$\frac{n}{V}$计算;
(2)①混合物中逐滴加入稀硫酸,Fe先和HNO3(氢离子由硫酸提供)生成NO,然后是Fe和H2SO4反应生成H2,据此确定溶液中的溶质;
②m1-m2的值为加入硫酸后再溶解的金属铁的质量,根据反应方程式中铁和硝酸根离子量的关系计算即可.
解答 解:(1)①容器中剩有m1 g的铁粉,所得溶液中的溶质为Fe(NO3)2,
故答案为:Fe(NO3)2;
②硝酸完全反应生成硝酸亚铁与NO,NO的物质的量=$\frac{0.672L}{22.4L/mol}$=0.03mol,根据电子转移守恒,参加反应的n(Fe)=$\frac{0.03mol×3}{2}$=0.045mol,由氮元素守恒可知:n(HNO3)=2n[Fe(NO3)2]+n(NO)=2×0.045mol+0.03mol=0.12mol,故原硝酸的物质的量浓度=$\frac{0.12mol}{0.2L}$=0.6mol/L,
故答案为:0.6;
(2)①向上述固-液混合物中逐滴加入稀硫酸溶液中的反应顺序为:Fe先和HNO3(氢离子由硫酸提供)生成NO,因为此时铁还是有剩余,所以硝酸根离子被消耗光,硝酸根反应完全后,再是Fe和H2SO4反应生成H2,此时溶液中的溶质为硫酸亚铁,
故答案为:FeSO4;
②Fe先和HNO3(氢离子由硫酸提供)生成NO,关系为:3Fe~2NO3-,溶液中硝酸根离子的物质的量是0.12mol-0.03mol=0.09mol,所以消耗铁的物质的量是$\frac{0.09mol×3}{2}$=0.135mol,质量是0.135mol×56g/mol=7.56≈7.6g,即m1-m2 的值为 7.6,
故答案为:7.6;
点评 本题考查化学方程式的计算、氧化还原反应计算,侧重对解题方法技巧与学生分析解决问题能力的考查,注意根据守恒进行解答,难度较大.

| A. | 浓氨水检验泄露的氯气,产生白烟:2NH3+3Cl2═6HCl+N2 | |
| B. | 铁氰化钾检验溶液中Fe2+,产生蓝色沉淀:3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓ | |
| C. | 浓溴水检验水体中的苯酚,产生白色沉淀: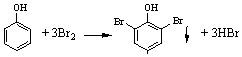 | |
| D. | 新制Cu(OH)2检验产品中乙醛,产生砖红色沉淀:CH3CHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$CH3COONa+Cu2O↓+3H2O |
| A. | 盐酸 | B. | 食盐 | C. | 液氯 | D. | 酒精 |
| A. | 72.4% | B. | 75% | C. | 50% | D. | 80.5% |
| A. | 沸点:乙烷>甲烷 | |
| B. | 二氯甲烷有两种不同结构的同分异构体 | |
| C. | 乙二醇和丙三醇为同系物 | |
| D. | 甲苯的一氯代物有三种 |
| A. | 食盐 | B. | 蔗糖 | C. | 香料 | D. | 福尔马林 |
| A. | 过氧化钠投入水中:Na2O2+H2O═2Na++2OH-+O2↑ | |
| B. | 烧碱溶液吸收氯气:Cl2+2OH═Cl-+ClO-+H2O | |
| C. | 碳酸钙溶于盐酸:CO32-+2H+═H2O+CO2↑ | |
| D. | 向氯化亚铁溶液中滴入氯水:Fe2++Cl2═Fe3++2Cl- |
| X | Y | Z | |
| W | Q | M |
| A. | 对应氢化物的沸点Y>Q是因为Y的非金属性比Q强 | |
| B. | XM4的比例模型为  其二氢取代物有两种 其二氢取代物有两种 | |
| C. | W的氧化物,常温下可以和Z、M的氢化物反应 | |
| D. | Z的单质能将Y的单质从其氢化物中置换出来 |