题目内容
8.X、Y、Z、W、R五种短周期元素原子序数依次增大,X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,其氢氧化物能溶于强碱溶液但不溶于氨水,W单质是人类将太阳能转变为电能的常用材料,下列相关说法正确的是( )| A. | W的最高价氧化物对应的水化物难溶于水 | |
| B. | 原子半径按X、Y、Z、R、W的顺序依次增大 | |
| C. | Z与Y形成的化合物是碱性氧化物 | |
| D. | WY2能与强碱溶液反应,但不能与任何酸反应 |
分析 X、Y、Z、W、R五种短周期元素原子序数依次增大,X原子是所有原子中半径最小的,则X为H元素,Y原子的最外层电子数是次外层的3倍,则Y有2个电子层,最外层电子数为6,故Y为O元素,Y、R同主族,故R为S元素,Z、W、R同周期,即处于第三周期,Z是常见的金属,其氢氧化物能溶于强碱溶液但不溶于氨水,则Z为Al,W单质是人类将太阳能转变为电能的常用材料,则W为Si.
解答 解:X、Y、Z、W、R五种短周期元素原子序数依次增大,X原子是所有原子中半径最小的,则X为H元素,Y原子的最外层电子数是次外层的3倍,则Y有2个电子层,最外层电子数为6,故Y为O元素,Y、R同主族,故R为S元素,Z、W、R同周期,即处于第三周期,Z是常见的金属,其氢氧化物能溶于强碱溶液但不溶于氨水,则Z为Al,W单质是人类将太阳能转变为电能的常用材料,则W为Si.
A.W的最高价氧化物对应的水化物为硅酸,难溶于水,故A正确;
B.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故半径X(H)<Y(O)<R(S)<W(Si)<Z(Al),故B错误;
C.Z与Y形成的化合物是氧化铝,属于两性氧化物,故C错误;
D.SiO2能与强碱溶液反应,能与氢氟酸反应,故D错误.
故选:A.
点评 本题考查了结构性质位置关系、元素周期律、元素化合物的性质等,推断元素是解题的关键,注意基础知识的掌握,难度不大.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
18.a、b、c、d为短周期元素,a的M电子层有1个电子,b的最外层电子数为内层电子数的2倍,c的最高化合价为最低化合价绝对值的3倍,c与d同周期,d的原子半径小于c.下列叙述错误的是( )
| A. | d元素的非金属性最强 | |
| B. | 它们均存在两种或两种以上的氧化物 | |
| C. | a可与c、d元素分别形成离子化合物 | |
| D. | b、c、d在化学反应中均易得到电子 |
19.下列物质中,不能用作漂白剂的是( )
| A. | SO2 | B. | Ca(ClO)2 | C. | NaClO | D. | HCl |
16.下列叙述能证明金属A的金属性比金属B强的是( )
| A. | A原子的最外层电子数比B原子最外层电子数少 | |
| B. | 常温下,A能从冷水中置换出氢气,而B不能 | |
| C. | 等物质的量A和B与足量稀硫酸反应,产生氢气的量A比B多 | |
| D. | A原子的电子层数比B原子电子层数多 |
3.对化学反应的速率和限度的叙述正确的是( )
| A. | 增加某一反应物的用量一定能够加快该反应的速率 | |
| B. | 化学反应的限度是不可改变的 | |
| C. | 化学反应进行的时间越长该反应的限度越大 | |
| D. | 化学反应达到限度时,正逆反应速率相等 |
13.下列有关物质的表达式正确的是( )
| A. | 乙烯的结构简式:CH2 CH2 | B. | 丙烯的球棍模型: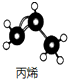 | ||
| C. | 醛基的结构简式:-COH | D. | 羟基的电子式: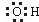 |
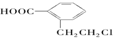 ,A在一定条件下有如图所示的转化关系.已知E分子式为C9H8O2.
,A在一定条件下有如图所示的转化关系.已知E分子式为C9H8O2.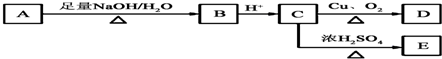
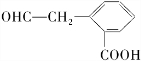 ,若E能使溴的四氯化碳溶液褪色,还能与NaHCO3溶液反应生成F,欲由A通过一步反应得到F,该反应的化学方程式是
,若E能使溴的四氯化碳溶液褪色,还能与NaHCO3溶液反应生成F,欲由A通过一步反应得到F,该反应的化学方程式是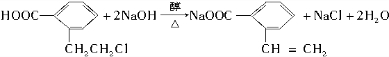 .
. ,写出所有符合下列要求的E的同分异构体的结构简式:
,写出所有符合下列要求的E的同分异构体的结构简式: 、
、 .
. NH4++OH-;实验室制备A的氢化物的化学方程式为Ca(OH)2+2NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2NH3↑+2H2O.
NH4++OH-;实验室制备A的氢化物的化学方程式为Ca(OH)2+2NH4Cl $\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2NH3↑+2H2O.