题目内容
18.根据原子结构及元素周期律的知识,下列推断正确的是( )| A. | 同主族元素含氧酸的酸性随核电荷数的增加而减弱 | |
| B. | 12C和石墨互为同素异形体 | |
| C. | Cl?、S2?、Ca2+、K+半径逐渐减小 | |
| D. | ${\;}_{17}^{35}$Cl与${\;}_{17}^{37}$Cl得电子能力相同 |
分析 A.同主族自上而下非金属性减弱,最高价含氧酸的酸性减弱;
B、同素异形体是单质之间,而不是核素间;
C、电子排布相同的微粒,原子序数越大,半径越小;
D、同位素的化学性质相同.
解答 解:A.同主族自上而下非金属性减弱,最高价含氧酸的酸性减弱,不是最高价含氧酸,则不一定,故A错误;
B、同素异形体是单质之间,而不是核素间,故B错误;
C、电子排布相同的微粒,原子序数越大,半径越小,则S2?、Cl?、K+、Ca2+半径逐渐减小,故C错误;
D、同位素的化学性质相同,35Cl与37Cl互为同位素,所以它们形成的单质的化学性质相同,即35Cl2与37Cl2得电子能力相同,故D正确.
故选:D.
点评 本题考查元素周期表的结构及应用,把握元素周期律、周期表中的族序数、原子序数等关系为解答的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列无色透明溶液,能大量共存的是( )
| A. | K+、Na+、Cl-、HCO3-、OH- | B. | Cl-、NO3-、MnO4-、K+、Na+ | ||
| C. | SO42-、K+、Mg2+、Cl-、NO3- | D. | H+、Cl-、Br-、HS-、K+ |
9.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11.2 L的戊烷所含的分子数为0.5NA | |
| B. | 0.5mol C3H8分子中含C-H共价键2NA | |
| C. | 11.2 L二氯甲烷所含分子数为0.5NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14 g,其原子数为3NA |
6.下列说法正确的是( )
| A. | 电解MgCl2饱和溶液,可制得金属镁 | |
| B. | 镀锡铁制品和镀锌铁制品的镀层破损时,镀锡铁中铁的腐蚀速率更快 | |
| C. | 在轮船船体四周镶嵌锌块保护船体不受腐蚀的方法叫牺牲阳极的阴极保护法 | |
| D. | 不锈钢有较强的抗腐蚀能力是因为在钢铁表面镀上了铬 |
3.下列有关说法中错误的是( )
| A. | CCl4可以由CH4制得,它可用于萃取碘水中的碘 | |
| B. | 相等的物质的量的乙烯和甲烷完全燃烧后产生的水的质量相同 | |
| C. | 用乙烯与HCl反应来制备氯乙烷比用乙烷与氯气反应更好 | |
| D. | 甲烷的空间构型是正四面体,所以二氯甲烷有两种不同的结构 |
4.短周期元素X、Y、Z、M、N原子序数依次增大,有关信息如下:
(1)XY2的电子式是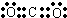 ;
;
Z2Y2中所含化学键类型是离子键和非极性共价键;(极性键、非极性键、离子键)
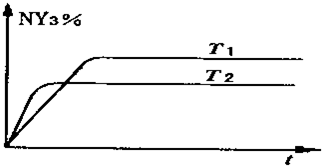
(2)①恒容条件下,一定量的NY2、Y2发生反应:2NY2(g)+Y2(g)?2NY3(g).
温度分别为T1和T2时,NY3的体积分数随时间变化如图,该反应的△H<0(填“>”“<”或“=”,下同)若T1、T2时刻反应的化学平衡常数分别为K1、K2,则K1>K2.
②恒压条件下,在该容器中充入惰性气体v(NY2)将减小(填增大或减小)
| 元素 | 有关信息 |
| X | 最外层电子数是次外层的2倍 |
| Y | 元素主要化合价为-2价 |
| Z | 其单质及化合物的焰色为黄色 |
| M | 与X同主族,其单质为半导体材料 |
| N | 其单质在Y单质中燃烧,发出明亮的蓝紫色火焰 |
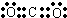 ;
;Z2Y2中所含化学键类型是离子键和非极性共价键;(极性键、非极性键、离子键)
(2)①恒容条件下,一定量的NY2、Y2发生反应:2NY2(g)+Y2(g)?2NY3(g).
温度分别为T1和T2时,NY3的体积分数随时间变化如图,该反应的△H<0(填“>”“<”或“=”,下同)若T1、T2时刻反应的化学平衡常数分别为K1、K2,则K1>K2.

②恒压条件下,在该容器中充入惰性气体v(NY2)将减小(填增大或减小)
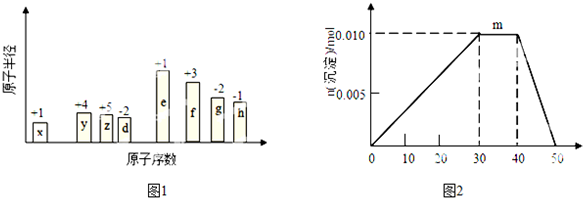
 (或
(或
 ).
).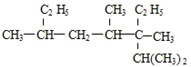 2,3,4,6-四甲基-3-乙基辛烷
2,3,4,6-四甲基-3-乙基辛烷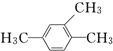 1,2,4-三甲苯
1,2,4-三甲苯