题目内容
5.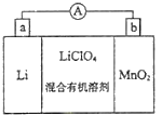 如图是锂锰电池的反应原理示意图,其中电解质KClO4溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO2晶格中,得到LiMnO2.回答下列问题:
如图是锂锰电池的反应原理示意图,其中电解质KClO4溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO2晶格中,得到LiMnO2.回答下列问题:(1)①外电路的电流方向是由b极流向a极.(填字母)
②电池正极反应式为Li++MnO2+e-=LiMnO2.
(2)用CR2032锂锰电池作电源分别电解以下三种溶液,假如电路中转移了0.4mol e-,且电解池的电极均为惰性电极.
①电解MNO3溶液时某一电极增加了43.2g M,则金属M的相对原子质量为108.
②电解含有0.4mol K2SO4的溶液100mL,恢复到原来的状态,需要进行的操作是(写出要加入的物质和质量)向溶液中加入3.6g水.
③电解含有0.2mol NaCl的溶液100mL,阳极产生的气体在标准状况下的体积是3.36L;将电解后的溶液加水稀释至2L,此时溶液的pH=13.
分析 (1)形成原电池反应时,Li为负极,被氧化,电极方程式为Li-e-=Li+,MnO2为正极,被还原,电极方程式为MnO2+e-+Li+=LiMnO2,结合电极方程式以及元素化合价的变化解答该题;
(2)①硝酸根离子为-1价,根据化合物中各元素化合价的代数和为0知,M元素在该化合物中化合价为+1价,电路中转移电子为0.4mol,则n(M)=n(e-)=0.4mol,M=$\frac{m}{n}$,数值上金属元素的摩尔质量等于其相对原子质量;
②根据“析出什么加入什么”原则加入物质,电解硫酸钾溶液时,阳极上析出氧气、阴极上析出氢气,所以相当于电解水,根据转移电子和析出物质之间的关系式计算;
③电解0.2molNaCl,氯离子完全放电转移电子物质的量为0.2mol,还有0.2mol电子是氢氧根离子转移的;电解过程分为两步:第一步电解反应式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑、第二步电解反应式为2H2O$\frac{\underline{\;通电\;}}{\;}$O2↑+2H2↑,根据c(NaOH)计算溶液pH.
解答 解:(1)①Li为负极,MnO2为正极,原电池工作时,外电路的电流方向从正极到负极,即从b极流向a极,
故答案为:b;a;
②MnO2为正极,被还原,电极方程式为MnO2+e-+Li+=LiMnO2,故答案为:Li++MnO2+e-=LiMnO2;
(2)①硝酸根离子为-1价,根据化合物中各元素化合价的代数和为0知,M元素在该化合物中化合价为+1价,电路中转移电子为0.4mol,则n(M)=n(e-)=0.4mol,M=$\frac{m}{n}$=$\frac{43.2g}{0.4mol}$=108g/mol,数值上金属元素的摩尔质量等于其相对原子质量为108,故答案为:108;
②根据“析出什么加入什么”原则加入物质,电解硫酸钾溶液时,阳极上析出氧气、阴极上析出氢气,所以相当于电解水,生成1mol水转移电子2mol电子,则转移0.4mol电子生成n(H2O)=$\frac{0.4mol}{2}$×18g/mol=3.6g,需要进行的操作是向溶液中加入3.6g水即可,故答案为:向溶液中加入3.6g水;
③电解0.2molNaCl,氯离子完全放电转移电子物质的量为0.2mol,根据Cl原子守恒得n(Cl2)=$\frac{1}{2}$n(NaCl)=$\frac{1}{2}$×0.2mol=0.1mol,还有0.2mol电子是氢氧根离子转移的,生成n(O2)=$\frac{0.2mol}{4}$=0.05mol,则阳极生成气体体积=(0.1+0.05)mol×22.4L/mol=3.36L;电解过程分为两步:第一步电解反应式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑、第二步电解反应式为2H2O$\frac{\underline{\;通电\;}}{\;}$O2↑+2H2↑,根据Na原子守恒得n(NaOH)=n(NaCl)=0.2mol,c(NaOH)=$\frac{0.2mol}{2L}$=0.1mol/L,则溶液pH=13,故答案为:3.36L;13.
点评 本题以电解原理为载体考查计算,为高频考点,明确各个电极上发生的反应是解本题关键,注意③题阳极产物成分及其物质的量,为易错点.

| A. | 水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| B. | 用澄清石灰水鉴别SO2 和CO2 | |
| C. | 将Fe(NO3)2 溶于稀盐酸,滴加KSCN 溶液没有颜色变化 | |
| D. | 透闪石的化学成分为Ca2Mg5Si8O22(OH)2 写成氧化物的形式为:2CaO•5MgO•8SiO2•H2O |

(1)如图甲,在硫酸型酸雨地区,不纯的铜制品发生电化学腐蚀,Cu发生氧化反应(填写“氧化”或“还原”),写出正极的电极反应式O2+4H++4e-=2H2O;
(2)如图乙,将螺旋状的铜丝在酒精灯上灼烧,铜丝变黑色,然后将红热的铜丝插入NH4Cl固体中,过一会取出,发现插入部分的黑色变为光亮的红色,查阅资料可知,该过程有N2生成,写出由黑色变为光亮红色过程的反应方程式2NH4Cl+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2↑+2HCl+3H2O;
II 在一个密闭容器中发生反应:mA(g)+nB(g)?pC(g)
(1)该反应未加催化剂的v-t图象如图丙,若其他条件不变,仅在反应前加入合适的催化剂,则其v-t图象如图丁所示.以下说法正确的是②③⑤ (填序号)
①a1>a2
②b1<b2
③t1>t2
④右图中阴影部分面积更大
⑤两图中阴影部分面积相等
(2)在一定温度和不同压强下达到平衡时,分别得到物质A的物质的量浓度如下表
| 压强p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol•L-1 | 0.08 | 0.20 | 0.44 |
②当压强从2×105加压到5×105时,平衡的移动方向是C.
A.朝正反应方向移动 B.朝逆反应方向移动 C.不移动 D.不能确定
③其他条件相同时,在上述三个压强下分别发生该反应.2×105 Pa时,A的转化率随时间变化如图2,请在图中补充画出压强分别为5×105 Pa 和1×106 Pa时,A的转化率随时间的变化曲线(请在图线上标出压强).
| A. | 在五水硫酸铜中滴加少量浓硫酸,固体颜色由蓝变白,说明浓硫酸具有吸水性 | |
| B. | 在未知试液中滴加BaCl2溶液得白色沉淀,取该白色沉淀加稀盐酸不溶解,说明原未知试液中含有SO42- | |
| C. | 在铜片上滴加少量稀硫酸,无明显现象,说明稀硫酸没有氧化性 | |
| D. | 某未知气体通入品红溶液中,品红溶液褪色,则原气体一定是 SO2 |
| A. | Na2CO3溶液(NaHCO3),加入适量的NaOH溶液 | |
| B. | Na2CO3溶液(Na2SO4),加入适量的Ba(OH)2溶液后过滤 | |
| C. | NaHCO3溶液(Na2CO3),通入过量的CO2气体 | |
| D. | Na2O2粉末(Na2O),将混合物在空气中加热 |
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | +4、-2 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.102 | 0.110 | 0.143 | 0.160 | 0.186 |
(1)E元素在周期表中位于第三周期VIA族.
(2)A、H、J对应离子的半径由大到小的顺序是(填离子符号)F->Na+>Al3+,A离子的结构示意图为
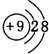 .
.(3)上述元素的最高价氧化物对应水化物的酸性最强的为S,碱性最强的为Na(填元素符号);这两种元素形成化合物的电子式为
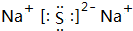 .
. | A. | 只含有1个双键的直链有机物 | B. | 含有2个双键的直链有机物 | ||
| C. | 含有1个双键的环状有机物 | D. | 含有1个叁键的直链有机物 |
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 放热反应在常温下一定很容易发生 | |
| C. | 反应是放热还是吸热,取决于反应物和生成物所具有的总能量的相对大小 | |
| D. | 在一定条件下,某可逆反应正向是吸热反应,则其逆向必是放热反应 |
 硫及其化合物广泛存在于自然界中,回答下列问题:
硫及其化合物广泛存在于自然界中,回答下列问题: