题目内容
10.W、X、Y、Z是原子序数依次增大的同一短周期主族元素,W、X是金属元素,Y、Z是非金属元素.W、X两者的最高价氧化物对应的水化物可以起反应生成盐和水.(1)W的名称是钠,上述反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(2)W与Y 可形成化合物W2Y,Y的离子结构示意图为
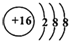 ,该化合物的电子式为
,该化合物的电子式为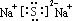 .
.(3)X与Z 可形成化合物是共价化合物而不是离子化合物,设计一个实验证明之:熔融状态不导电,则说明为共价化合物.
(4)Y的低价氧化物和Z的单质在水溶液中反应的化学方程式是:Cl2+SO2+2H2O=H2SO4+2HCl.
(5)Y 与Z能形成一种化合物,其所有原子都满足8电子结构,其分子式为SCl2或者S2Cl2.
分析 W、X、Y、Z是原子序数依次增大的同一短周期主族元素,W、X是金属元素,W、X两者的最高价氧化物对应的水化物可以起反应生成盐和水,可知W为Na,X为Al;Y、Z是非金属元素,结合(2)中W与Y 可形成化合物W2Y,可知Y为S,则Z为Cl,然后结合元素周期律及元素化合物知识来解答.
解答 解:W、X、Y、Z是原子序数依次增大的同一短周期主族元素,W、X是金属元素,W、X两者的最高价氧化物对应的水化物可以起反应生成盐和水,可知W为Na,X为Al;Y、Z是非金属元素,结合(2)中W与Y 可形成化合物W2Y,可知Y为S,则Z为Cl,
(1)W的名称是钠,上述反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,故答案为:钠;Al(OH)3+OH-=AlO2-+2H2O;
(2)W与Y 可形成化合物W2Y,YS,Y的离子结构示意图为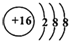 ,该化合物的电子式为
,该化合物的电子式为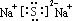 ,故答案为:
,故答案为: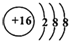 ;
;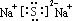 ;
;
(3)X与Z 可形成化合物是共价化合物而不是离子化合物,设计实验为熔融状态不导电,则说明为共价化合物,
故答案为:熔融状态不导电,则说明为共价化合物;
(4)Y的低价氧化物为二氧化硫,和Z的单质(氯气)在水溶液中发生氧化还原反应,反应的化学方程式是Cl2+SO2+2H2O=H2SO4+2HCl,
故答案为:Cl2+SO2+2H2O=H2SO4+2HCl;
(5)Y与Z能形成一种化合物,S最外层有6个电子,Cl最外层有7个电子,则其所有原子都满足8电子结构的分子式为SCl2 或者S2Cl2(其他合理答案如S3Cl2、S4Cl2等),故答案为:SCl2 或者S2Cl2.
点评 本题考查位置、结构及性质的综合应用,为高频考点,把握元素的位置、元素的性质推断元素为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识及周期律的应用,题目难度不大.

 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案| A. | 铜片、银片,FeCl3溶液 | B. | 铜片、石墨棒,硝酸银溶液 | ||
| C. | 锌片、铜片,稀盐酸 | D. | 铜片、石墨棒,稀硫酸 |
①Zn是负极
②Cu是正极
③负极反应:Zn-2e-=Zn2+
④正极反应:Cu2++2e-=Cu
⑤H+向负极移动
⑥电子由Cu极通过导线向Zn极移动.
| A. | 仅①②③⑤ | B. | ①②③④⑤ | C. | 仅②③④⑥ | D. | 仅①②③ |
| A. | 水的电子式: | B. | CH4分子的比例模型: | ||
| C. | 铝的原子结构示意图: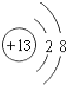 | D. | 乙烯的结构简式:CH2CH2 |
| A. | 27% | B. | 52% | C. | 40% | D. | 41.4% |

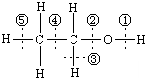 图为乙醇分子的化学键示意图,请按要求回答问题:
图为乙醇分子的化学键示意图,请按要求回答问题: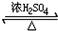 CH3COOCH2CH3+H2O,
CH3COOCH2CH3+H2O,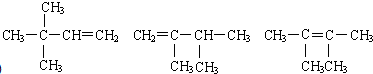 任意一种(写出其中一种即可).
任意一种(写出其中一种即可).