题目内容
用0.1000mol?L-1的HCl标准溶液滴定未知浓度的NaOH溶液,试根据实验回答下列问题:
A.移取10.00mL待测烧碱溶液注入洁净的锥形瓶,并加入2~3滴甲基橙
B.取一支酸式滴定管用蒸馏水洗净,再用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的酸式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D.取标准HCl溶液注入酸式滴定管至刻度“0”以上2~3mL;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准HCl溶液滴定至终点并记下滴定管液面的刻度.
(1)正确操作步骤的顺序是(用字母序号填写) .
(2)判断到达滴定终点的实验现象是 .
(3)下列操作中可能使所测NaOH溶液的浓度数值偏高的是 (填字母序号).
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时读数正确
E.量取NaOH溶液的碱式滴定管未用待测溶液润洗就直接注入待测溶液
(4)根据下表数据,计算被测烧碱溶液的物质的量浓度是 mol/L.
(5)在滴定过程中到达滴定终点时,不慎多滴加了一滴HCl溶液(1滴溶液的体积约为0.05mL),继续加水稀释至50mL,所得溶液的PH是 .
A.移取10.00mL待测烧碱溶液注入洁净的锥形瓶,并加入2~3滴甲基橙
B.取一支酸式滴定管用蒸馏水洗净,再用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的酸式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D.取标准HCl溶液注入酸式滴定管至刻度“0”以上2~3mL;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准HCl溶液滴定至终点并记下滴定管液面的刻度.
(1)正确操作步骤的顺序是(用字母序号填写)
(2)判断到达滴定终点的实验现象是
(3)下列操作中可能使所测NaOH溶液的浓度数值偏高的是
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时读数正确
E.量取NaOH溶液的碱式滴定管未用待测溶液润洗就直接注入待测溶液
(4)根据下表数据,计算被测烧碱溶液的物质的量浓度是
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
考点:中和滴定
专题:实验题
分析:(1)根据中和滴定有检漏、洗涤、润洗、装液、取待测液并加指示剂、滴定等操作;
(2)如溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
(3)根据c(待测)=
,分析不当操作对V(标准)的影响,以此判断浓度的误差;
(4)根据c(待测)=
计算,V(标准)用两次的平均值;
(5)根据稀释前后HCl的物质的量守恒计算.
(2)如溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
(3)根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
(4)根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
(5)根据稀释前后HCl的物质的量守恒计算.
解答:
解:(1)中和滴定按照检漏、洗涤、润洗、装液、取待测液并加指示剂、滴定等顺序操作,则正确的顺序为:B、D、C、E、A、F,
故答案为:B、D、C、E、A、F;
(2)本实验是用HCl滴定氢氧化钠溶液,用酚酞作指示剂,所以终点时,现象是当溶液由浅红色变为无色,且在半分钟内不恢复,
故答案为:溶液由浅红色变为无色,且半分钟内不恢复;
(3)A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液,标准液的浓度偏小,造成V(标准)偏大,根据c(待测)=
,可知c(标准)偏高,故A正确;
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥,待测液的物质的量不变,对V(标准)无影响,根据c(待测)=
,可知c(标准)不变,故B错误;
C.酸式滴定管在滴定前有气泡,滴定后气泡消失,造成V(标准)偏大,根据c(待测)=
,可知c(标准)偏高,故C正确;
D.读取盐酸体积时,开始仰视读数,滴定结束时正确,造成V(标准)偏小,根据c(待测)=
,可知c(标准)偏小,故D错误;
E.量取NaOH溶液的碱式滴定管未用待测溶液润洗就直接注入待测溶液,则氢氧化钠的浓度减小,所以滴定时消耗的盐酸的体积偏小,即标准溶液的体积偏小,根据c(待测)=
,可知c(标准)偏小,故E错误;
故答案为:AC;
(4)V(标准)=
mL=20.00mL,
c(待测)=
=
=0.2000mol?L-1,
故答案为:0.2000;
(5)已知0.1000mol?L-1的HCl,多加一滴,1滴溶液的体积约为0.05mL,滴定后,继续加水稀释至50mL,
则0.1000mol?L-1×0.05mL=c×50mL,解得c=10-4mol/L,所以溶液中氢离子的浓度为10-4mol/L,则溶液的pH=4,
故答案为:4.
故答案为:B、D、C、E、A、F;
(2)本实验是用HCl滴定氢氧化钠溶液,用酚酞作指示剂,所以终点时,现象是当溶液由浅红色变为无色,且在半分钟内不恢复,
故答案为:溶液由浅红色变为无色,且半分钟内不恢复;
(3)A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液,标准液的浓度偏小,造成V(标准)偏大,根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥,待测液的物质的量不变,对V(标准)无影响,根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
C.酸式滴定管在滴定前有气泡,滴定后气泡消失,造成V(标准)偏大,根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
D.读取盐酸体积时,开始仰视读数,滴定结束时正确,造成V(标准)偏小,根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
E.量取NaOH溶液的碱式滴定管未用待测溶液润洗就直接注入待测溶液,则氢氧化钠的浓度减小,所以滴定时消耗的盐酸的体积偏小,即标准溶液的体积偏小,根据c(待测)=
| V(标准)×c(标准) |
| V(待测) |
故答案为:AC;
(4)V(标准)=
| (20.50-0.40)+(24.00-4.10) |
| 2 |
c(待测)=
| V(标准)×c(标准) |
| V(待测) |
| 0.1000mol/L×20.00mL |
| 10.00mL |
故答案为:0.2000;
(5)已知0.1000mol?L-1的HCl,多加一滴,1滴溶液的体积约为0.05mL,滴定后,继续加水稀释至50mL,
则0.1000mol?L-1×0.05mL=c×50mL,解得c=10-4mol/L,所以溶液中氢离子的浓度为10-4mol/L,则溶液的pH=4,
故答案为:4.
点评:本题考查了中和滴定操作及误差分析,操作时要规范,分析误差时要看是否影响标准体积的用量,本题难度中等.

练习册系列答案
相关题目
关于下列图象说法不正确的是( )
A、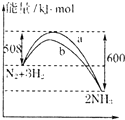 表示的热化学方程式为:N2(g)+3H2(g)═2NH3(g);△H=-92kJ.mol-1 表示的热化学方程式为:N2(g)+3H2(g)═2NH3(g);△H=-92kJ.mol-1 |
B、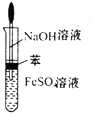 表示实验室中制取Fe(OH)2沉淀,可以防Fe(OH)2被氧比 表示实验室中制取Fe(OH)2沉淀,可以防Fe(OH)2被氧比 |
C、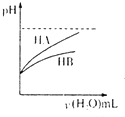 表示常温下稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB 表示常温下稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB |
D、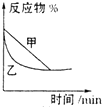 表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 |
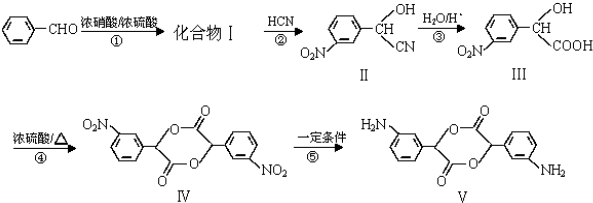
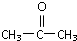 )代替化合物 I发生反应②和反应③可以得到化合物Ⅵ(生产有机玻璃的中间体),则化合物Ⅵ的结构简式为
)代替化合物 I发生反应②和反应③可以得到化合物Ⅵ(生产有机玻璃的中间体),则化合物Ⅵ的结构简式为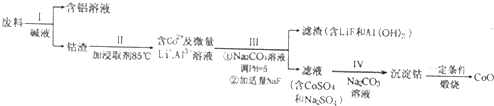
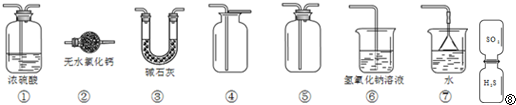
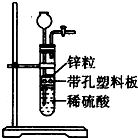 某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足而又无其他酸液可加入.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的①NaN03溶液②酒精③四氯化碳 ④苯⑤Na2C03溶液⑥KCl溶液.( )
某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足而又无其他酸液可加入.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的①NaN03溶液②酒精③四氯化碳 ④苯⑤Na2C03溶液⑥KCl溶液.( )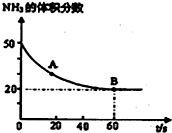 氮的化合物是一把双刃剑,它既是一种资源,又会给环境造成危害.
氮的化合物是一把双刃剑,它既是一种资源,又会给环境造成危害.