题目内容
13.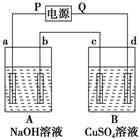 按图中装置实验,A、B两烧杯分别盛放200g 10% NaOH溶液和足量CuSO4溶液.通电一段时间后,c极上有Cu析出,又测得电路通过电子0.5mol,试回答:
按图中装置实验,A、B两烧杯分别盛放200g 10% NaOH溶液和足量CuSO4溶液.通电一段时间后,c极上有Cu析出,又测得电路通过电子0.5mol,试回答:(1)电源的P极为负极.
(2)b极产生气体的体积为2.8L(标准状况).
(3)c极增加的质量为16g.
(4)d极上所发生的电极反应式为:4OH--4e-=2H2O+O2↑.
分析 c极上有Cu析出,说明c为电解池的阴极,d为阳极,则P为负极,Q为正极,A为电解NaOH溶液,实质上为电解水,其中a为阴极,b为阳极,B为电解硫酸铜溶液,在阴极析出铜,电极反应:Cu2++2e-=Cu,阳极生成氧气,发生4OH--4e-=2H2O+O2↑,结合电极方程式计算.
解答 解:(1)c极上有Cu析出,说明c为电解池的阴极,d为阳极,则P为负极,故答案为:负;
(2)b为阳极,发生4OH--4e-=2H2O+O2↑,电路通过电子0.5mol,则生成0.125mol氧气,体积为0.125mol×22.4L/mol=2.8L,故答案为:2.8;
(3)电子转移为0.5mol;C电极析出的是铜,由电极反应Cu2++2e-═Cu,计算得到生成铜物质的量为0.25mol,质量=0.25mol×64g/mol=16g;
故答案为:16g;
(4)d电极是阳极,阳极上氢氧根离子放电生成氧气,电极反应式为4OH--4e-=2H2O+O2↑,故答案为:4OH--4e-=2H2O+O2↑.
点评 本题为电化学知识的综合应用,做题时要注意根据电极反应现象判断出电解池的阴阳级,进而判断出电源的正负极,要注意三个电解池为串联电路,各电极上得失电子的数目相等.做题时要正确写出电极方程式,准确判断两极上离子的放电顺序.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
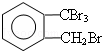
4.以CH3CH2CH2Cl为原料制取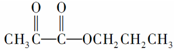 ,最简便的流程需要下列反应的顺序是
,最简便的流程需要下列反应的顺序是
a:氧化 b:还原 c:取代 d:加成 e:消去 f:中和 g:加聚 h:酯化( )
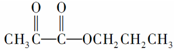 ,最简便的流程需要下列反应的顺序是
,最简便的流程需要下列反应的顺序是a:氧化 b:还原 c:取代 d:加成 e:消去 f:中和 g:加聚 h:酯化( )
| A. | b d f g h | B. | e a d c h | C. | b a e c h | D. | e d c a h |
1.下列分子中,所有原子都处于同一平面上的是( )
| A. | 丁烯 | B. | 丙炔 | C. | 乙烷 | D. | 苯 |
8.化学键的键能是指气态原子间形成1mol化学键时释放的能量.如H-I键的键能为297KJ•mol-1,也可以理解为破坏1mol H-I键需要吸收297KJ的热量.一个化学反应一般都有旧化学键的破坏和新化学键的形成.
下表是一些键能数据(KJ•mol-1):
回答下列问题:
由表中数据能否得出这样的结论:
(1)半径越小的原子形成的共价键越牢固(即键能越大)不能(填“能”或“不能”)
(2)非金属性越强的原子形成的共价键越牢固不能(填“能”或“不能”).能否从数据找出一些规律,请写出一条:与相同原子结合时同主族元素形成的共价键,原子半径越小,共价键越强;
(3)试预测C-Br键的键能范围218KJ•mol-1<C-Br键能<330KJ•mol-1.
下表是一些键能数据(KJ•mol-1):
| 键能 | 键能 | 键能 | 键能 | ||||
| H-H | 436 | Cl-Cl | 243 | H-Cl | 432 | H-O | 464 |
| S=S | 255 | H-S | 339 | C-F | 427 | C-O | 347 |
| C-Cl | 330 | C-I | 218 | H-F | 565 |
由表中数据能否得出这样的结论:
(1)半径越小的原子形成的共价键越牢固(即键能越大)不能(填“能”或“不能”)
(2)非金属性越强的原子形成的共价键越牢固不能(填“能”或“不能”).能否从数据找出一些规律,请写出一条:与相同原子结合时同主族元素形成的共价键,原子半径越小,共价键越强;
(3)试预测C-Br键的键能范围218KJ•mol-1<C-Br键能<330KJ•mol-1.
2.下列不能使碘化钾淀粉试纸变蓝的物质是( )
| A. | 溴水 | B. | 溴化钠 | C. | 氯水 | D. | 碘水 |
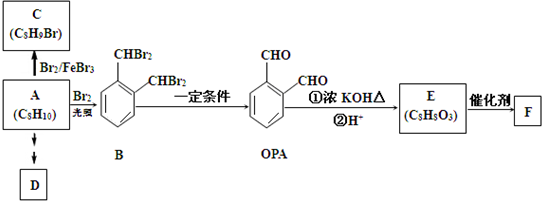

 ;
; ;
; .
.
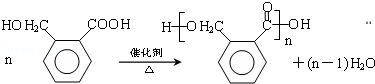 .
.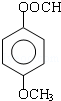 .
.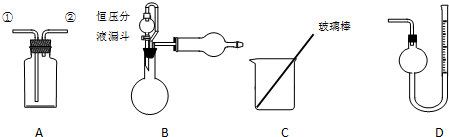
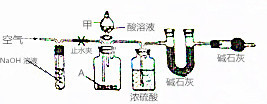 碱式碳酸盐A可用作胃药,其组成可表示为Al2Mg6(OH)x(CO3)y•zH2O.某校化学兴趣小组欲测定其化学式,实验设计如下:
碱式碳酸盐A可用作胃药,其组成可表示为Al2Mg6(OH)x(CO3)y•zH2O.某校化学兴趣小组欲测定其化学式,实验设计如下: