题目内容
 氨在国民经济中占有重要地位.
氨在国民经济中占有重要地位.(1)合成氨工业中,合成塔中每产生2mol NH3,放出92.2kJ热量.工业合成氨的热化学方程式是
(2)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(l),该反应的平衡常数和温度关系如下:
| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)
| n(NH3) |
| n(CO2) |
③图中的B点处,NH3的平衡转化率为
考点:转化率随温度、压强的变化曲线,化学平衡建立的过程
专题:化学平衡专题
分析:(1)根据热化学方程式的意义和书写方法来回答判断;
(2)①依据平衡常数随温度变化分析判断反应吸热放热;
②增大反应物浓度,平衡正向进行;
③依据x含义和图象数据分析结合化学方程式换算氨气转化率.
(2)①依据平衡常数随温度变化分析判断反应吸热放热;
②增大反应物浓度,平衡正向进行;
③依据x含义和图象数据分析结合化学方程式换算氨气转化率.
解答:
解:(1)合成塔中每产生2mol NH3,放出92.2kJ热量,即N2(g)+3H2(g)?2NH3(g)△H=-92.2 kJ?mol-1,故答案为:N2(g)+3H2(g)?2NH3(g)△H=-92.2 kJ?mol-1;
(2)①平衡常数随温度升高减小,说明正反应为放热反应,△H<0,故答案为:<;
②2NH3 (g)+CO2 (g)?CO(NH2)2 (l)+H2O (l),图象分析判断,增大氨气浓度平衡正向进行,二氧化碳转化率增大,
故答案为:NH3的量增大,平衡正向移动,则增大CO2的转化率;
③B点处x=4,原料气中的NH3和CO2的物质的量之比为4,二氧化碳转化率为64%,假设氨气为4mol,二氧化碳为1mol,则反应的二氧化碳为0.64mol,
依据化学方程式2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(l)反应的氨气为1.28mol,
NH3的平衡转化率=
×100%=32%,
故答案为:32%.
(2)①平衡常数随温度升高减小,说明正反应为放热反应,△H<0,故答案为:<;
②2NH3 (g)+CO2 (g)?CO(NH2)2 (l)+H2O (l),图象分析判断,增大氨气浓度平衡正向进行,二氧化碳转化率增大,
故答案为:NH3的量增大,平衡正向移动,则增大CO2的转化率;
③B点处x=4,原料气中的NH3和CO2的物质的量之比为4,二氧化碳转化率为64%,假设氨气为4mol,二氧化碳为1mol,则反应的二氧化碳为0.64mol,
依据化学方程式2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(l)反应的氨气为1.28mol,
NH3的平衡转化率=
| 1.28mol |
| 4mol |
故答案为:32%.
点评:本题考查了化学能与热能关系分析判断,热化学方程式书写,化学平衡移动原理,题目难度中等.

练习册系列答案
相关题目
 如图所示装置中加入一定的铁粉,分液漏斗中加入一定体积浓度为l2mol?L-1的HNO3,加热并打开分液漏斗的活塞,使其充分反应后,下列微粒在该装置中一定大量存在的是( )
如图所示装置中加入一定的铁粉,分液漏斗中加入一定体积浓度为l2mol?L-1的HNO3,加热并打开分液漏斗的活塞,使其充分反应后,下列微粒在该装置中一定大量存在的是( )①NO3- ②Fe3+③H+④NO ⑤NO2.
| A、①⑤ | B、① |
| C、②④⑤ | D、①②④⑤ |
下列有机物的名称一定错误的是( )
| A、2一甲基一1一丁烯 |
| B、2,2一 二甲基丙烷 |
| C、5,5一二甲基一3一己烯 |
| D、4一甲基一2一戊炔 |
 :
: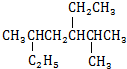 :
: :
: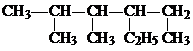 的名称是
的名称是 化合物A中含氧官能团的名称
化合物A中含氧官能团的名称