题目内容
己知X、Y、Z、W、N、U、V是短周期的主族元素,原子序数依次增大.X与N同主族,且与W都能形成A2B、A2B2型化合物;Z、W的单质常温下均为无色气体;Y原子的L层电子数是K层电子数的2倍;U原子的最外层电子数是其电子层数的2倍,试回答下列问题:
(1)YW2的电子式 ;V原子的结构示意图 ;Z的氢化物结构式为 ;写出U元素在周期表中的位置 ;N2W2中含有的化学键有 (化学键类型)
(2)X、Y、Z、W四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物,该化合物的稀溶液与足量氢氧化钠溶液反应的离子方程式为 .
(3)写出UW2与V元素的单质在水溶液中反应的化学方程式是 .
(1)YW2的电子式
(2)X、Y、Z、W四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物,该化合物的稀溶液与足量氢氧化钠溶液反应的离子方程式为
(3)写出UW2与V元素的单质在水溶液中反应的化学方程式是
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W、N、U、V是短周期的主族元素,原子序数依次增大,Y原子的L层电子数是K层电子数的2倍,则Y核外电子数=2+4=6,所以Y是C元素;
Z、W的单质常温下均为无色气体,且原子序数大于Y,所以Z是N元素、W是O元素;
X与N同主族,且与W都能形成A2B、A2B2型化合物,X原子序数小于N,在X是H元素、N是Na元素;
U原子的最外层电子数是其电子层数的2倍,其最外层电子数是6,且原子序数大于11,所以U是S元素;
V是短周期主族元素,其原子序数大于U,所以V是Cl元素,
再结合物质的结构性质解答.
Z、W的单质常温下均为无色气体,且原子序数大于Y,所以Z是N元素、W是O元素;
X与N同主族,且与W都能形成A2B、A2B2型化合物,X原子序数小于N,在X是H元素、N是Na元素;
U原子的最外层电子数是其电子层数的2倍,其最外层电子数是6,且原子序数大于11,所以U是S元素;
V是短周期主族元素,其原子序数大于U,所以V是Cl元素,
再结合物质的结构性质解答.
解答:
解:X、Y、Z、W、N、U、V是短周期的主族元素,原子序数依次增大,Y原子的L层电子数是K层电子数的2倍,则Y核外电子数=2+4=6,所以Y是C元素;
Z、W的单质常温下均为无色气体,且原子序数大于Y,所以Z是N元素、W是O元素;
X与N同主族,且与W都能形成A2B、A2B2型化合物,X原子序数小于N,在X是H元素、N是Na元素;
U原子的最外层电子数是其电子层数的2倍,其最外层电子数是6,且原子序数大于11,所以U是S元素;
V是短周期主族元素,其原子序数大于U,所以V是Cl元素,
(1)CO2的电子式为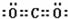 ;V是Cl元素,其原子核外有3个电子层、最外层电子数是7,则Cl原子的结构示意图为
;V是Cl元素,其原子核外有3个电子层、最外层电子数是7,则Cl原子的结构示意图为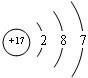 ;Z是N元素,氮元素氢化物的结构式为
;Z是N元素,氮元素氢化物的结构式为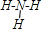 ;U是S元素,S元素在周期表中的位置是第三周期第VIA族;Na2O2中钠离子和过氧根离子之间存在离子键、O原子和O原子之间存在共价键,所以过氧化钠中含有的化学键有离子键和共价键,
;U是S元素,S元素在周期表中的位置是第三周期第VIA族;Na2O2中钠离子和过氧根离子之间存在离子键、O原子和O原子之间存在共价键,所以过氧化钠中含有的化学键有离子键和共价键,
故答案为: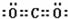 ;
; ;
;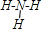 ;第三周期第VIA族;离子键和共价键;
;第三周期第VIA族;离子键和共价键;
(2)H、C、N、O四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物为NH4HCO3,该化合物的稀溶液与足量氢氧化钠溶液反应生成碳酸钠、水和一水合氨,离子方程式为NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O,故答案为:NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O;
(3)SO2与氯气在水溶液中发生氧化还原反应生成盐酸和硫酸,化学方程式是SO2+Cl2+2H2O=2HCl+H2SO4,故答案为:SO2+Cl2+2H2O=2HCl+H2SO4.
Z、W的单质常温下均为无色气体,且原子序数大于Y,所以Z是N元素、W是O元素;
X与N同主族,且与W都能形成A2B、A2B2型化合物,X原子序数小于N,在X是H元素、N是Na元素;
U原子的最外层电子数是其电子层数的2倍,其最外层电子数是6,且原子序数大于11,所以U是S元素;
V是短周期主族元素,其原子序数大于U,所以V是Cl元素,
(1)CO2的电子式为
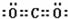 ;V是Cl元素,其原子核外有3个电子层、最外层电子数是7,则Cl原子的结构示意图为
;V是Cl元素,其原子核外有3个电子层、最外层电子数是7,则Cl原子的结构示意图为 ;Z是N元素,氮元素氢化物的结构式为
;Z是N元素,氮元素氢化物的结构式为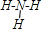 ;U是S元素,S元素在周期表中的位置是第三周期第VIA族;Na2O2中钠离子和过氧根离子之间存在离子键、O原子和O原子之间存在共价键,所以过氧化钠中含有的化学键有离子键和共价键,
;U是S元素,S元素在周期表中的位置是第三周期第VIA族;Na2O2中钠离子和过氧根离子之间存在离子键、O原子和O原子之间存在共价键,所以过氧化钠中含有的化学键有离子键和共价键,故答案为:
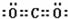 ;
; ;
;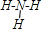 ;第三周期第VIA族;离子键和共价键;
;第三周期第VIA族;离子键和共价键;(2)H、C、N、O四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物为NH4HCO3,该化合物的稀溶液与足量氢氧化钠溶液反应生成碳酸钠、水和一水合氨,离子方程式为NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O,故答案为:NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O;
(3)SO2与氯气在水溶液中发生氧化还原反应生成盐酸和硫酸,化学方程式是SO2+Cl2+2H2O=2HCl+H2SO4,故答案为:SO2+Cl2+2H2O=2HCl+H2SO4.
点评:本题考查了元素位置结构性质的相互关系及应用,涉及氧化还原反应、化学用语、离子反应等知识点,根据原子结构、元素周期表结构确定元素是解本题关键,再结合物质的性质、结构分析解答,注意:碳酸氢铵和氢氧化钠的反应方程式与反应物的量有关,为易错点.

练习册系列答案
相关题目
在某一化学反应A+2B?3C中,生成物B的浓度在10s内从1.5mol/L变成2.0mol/L,则这10s内用生成物C的浓度变化表示的化学反应速率为( )
| A、0.05mol/(L?s) |
| B、0.05mol/L |
| C、0.033 mol/(L?s) |
| D、0.075 mol/(L?s) |
下列离子方程式中正确的是( )
| A、NaHSO4溶液和Ba(OH)2溶液充分反应后溶液呈中性:Ba2++2OH-+2H++SO4_2-=BaSO4↓+2H2O |
| B、向NH4Al(SO4)2溶液中滴入Ba(OH)2恰好使SO42-反应完全:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O |
| C、次氯酸钠溶液中通入SO2气体:2ClO-+SO2+H2O═2HClO+SO42- |
| D、Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O |
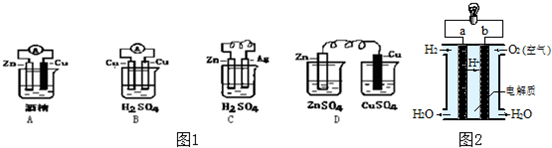
 将反应Cu+2FeCl3=CuCl2+2FeCl2设计成原电池,在图框中画出原电池的装置图,标出正、负极,并写出电极反应式.
将反应Cu+2FeCl3=CuCl2+2FeCl2设计成原电池,在图框中画出原电池的装置图,标出正、负极,并写出电极反应式. 某同学用固体NaOH配制1000mL 0.40mol/L的NaOH溶液,回答下列问题:
某同学用固体NaOH配制1000mL 0.40mol/L的NaOH溶液,回答下列问题: