题目内容
17.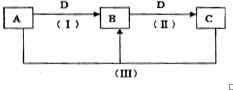 A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去).根据题意回答下列问题:
A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去).根据题意回答下列问题:(1)若A、B、C的焰色反应均为黄色,C为厨房的用品,D的过度排放会造成温室效应.
①A的化学式NaOH,
②反应Ⅱ的离子方程式是CO32-+CO2+H2O=2HCO3-,
③反应Ⅲ的离子方程式是HCO3-+OH-=CO32-+H2O,
(2)若A、D均为单质,且A为气体,D元素的一种红棕色氧化物常用作颜料.
①反应Ⅱ的离子方程式是Fe+2Fe3+=3Fe3+,
②反应Ⅲ的离子方程式是Cl2+2Fe+=2Fe3++2Cl-,
③写出以A为原料制取漂白粉的化学方程式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,
④检验B中阳离子的方法取少量B的溶液于试管中,向其中滴加KSCN溶液,若出现红色,说明B中阳离子为Fe3+.
分析 A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,
(1)若A、B、C的焰色反应均为黄色,均含有Na元素,C为厨房中的用品,则C为NaCl,D的过度排放会造成温室效应,D为CO2,A能与二氧化碳反应生成B,B能与二氧化碳反应生成C,B为碳酸钠,且A与C反应得到B,则A为NaOH、C为NaHCO3,据此解答;
(2)若A、D均为单质,D元素的一种红棕色氧化物常用作颜料,为Fe2O3,则D为Fe,且A为气体,由转化关系可知A具有强氧化性,将Fe氧化为高价态,可推知A为Cl2、B为FeCl3、C为FeCl2,据此解答.
解答 解:A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,
(1)若A、B、C的焰色反应均为黄色,均含有Na元素,C为厨房中的用品,则C为NaCl,D的过度排放会造成温室效应,D为CO2,A能与二氧化碳反应生成B,B能与二氧化碳反应生成C,B为碳酸钠,且A与C反应得到B,则A为NaOH、C为NaHCO3,
①由上述分析可知,A的化学式为NaOH,
故答案为:NaOH;
②反应II的离子方程式是:CO32-+CO2+H2O=2HCO3-,
故答案为:CO32-+CO2+H2O=2HCO3-;
③反应Ⅲ的离子方程式是HCO3-+OH-=CO32-+H2O,
故答案为:HCO3-+OH-=CO32-+H2O;
(2)若A、D均为单质,D元素的一种红棕色氧化物常用作颜料,为Fe2O3,则D为Fe,且A为气体,由转化关系可知A具有强氧化性,将Fe氧化为高价态,可推知A为Cl2、B为FeCl3、C为FeCl2,
①反应Ⅱ的离子方程式是:Fe+2Fe3+=3Fe3+,
故答案为:Fe+2Fe3+=3Fe3+;
②反应Ⅲ的离子方程式是:Cl2+2Fe+=2Fe3++2Cl-,
故答案为:Cl2+2Fe+=2Fe3++2Cl-;
③以氯气与氢氧化钙反应制备漂白粉,反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
④B中含有阳离子为Fe3+,检验方法是:取少量B的溶液于试管中,向其中滴加KSCN溶液,若出现红色,说明B中阳离子为Fe3+,
故答案为:取少量B的溶液于试管中,向其中滴加KSCN溶液,若出现红色,说明B中阳离子为Fe3+.
点评 本题考查无机物推断,涉及Na、Fe等元素单质化合物的性质与转化,物质的颜色是推断突破口,再结合转化关系推断,难度不大.

 阅读快车系列答案
阅读快车系列答案| A. | ①②④⑤ | B. | 仅②⑤ | C. | 仅②④⑤ | D. | ③④⑤ |
| A. | 铝的氧化物可用作于耐高温材料 | B. | Na2O2可用作漂白剂 | ||
| C. | 碱石灰可用于干燥CO2、O2等气体 | D. | 小苏打可用于治疗胃酸过多 |
| A. | H2燃烧热为285.8 kJ•mol-1,则2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1 | |
| B. | 若C(石墨,s)=C(金刚石,s)△H>0,则石墨比金刚石稳定 | |
| C. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4 kJ•mol-1,则0.5mol NaOH固体与稀盐酸完全中和,放出28.7kJ的热量 | |
| D. | 已知2SO2(g)+O2(g)?2SO2 (g)△H=-196.64 kJ•mol-1,在一定温度下,向一固定体积的密闭容器中通入2mol SO2、1mol O2,达到平衡时放出热量小于196.64 kJ |
请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含离子的化学组分及其浓度如下表:
| 离子 | H+ | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 未测定 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)为减少SO2的排放,常采取的措施有:①将煤转化为清洁气体燃料.
已知:2H2(g)+O2(g)═2H2O(g) K12C(s)+O2(g)=2CO (g) K2
2C(s)+2H2O(g)═2CO(g)+2H2(g)则K=$\sqrt{\frac{{K}_{2}}{{K}_{1}}}$(用含K1、K2的式子表示).
②洗涤含SO2的烟气.以下物质可作洗涤剂的是ab.
A.Ca(OH)2 B.Na2CO3 C.CaCl2D.NaHSO3
(3)汽车尾气中有NOx和CO的生成及转化,已知汽缸中生成NO的反应为:N2(g)+O2(g)?2NO(g)△H>0目前,在汽车尾气系统中装置催化转化器可减少CO和NOx的污染,其化学反应方程式为2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2.
| A. | Al→[Al(OH)4]- | B. | Na2CO3→NaOH | C. | Al2O3→Al(OH)3 | D. | Fe(OH)2→Fe(OH)3 |
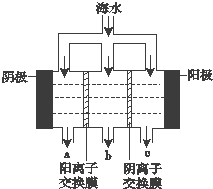 《科学》曾评出10大科技突破,其中“火星上‘找’到水的影子”名列第一.水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水质优劣直接影响人体健康.海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景.人类把海水淡化,就可以得到大量的饮用水,常规蒸馏法,技术和工艺比较完备,但也存在较大缺陷,大量推广离子交换法和电渗析法.
《科学》曾评出10大科技突破,其中“火星上‘找’到水的影子”名列第一.水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水质优劣直接影响人体健康.海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景.人类把海水淡化,就可以得到大量的饮用水,常规蒸馏法,技术和工艺比较完备,但也存在较大缺陷,大量推广离子交换法和电渗析法.