题目内容
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、使甲基橙变红的溶液:K+、Na+、SO42-、CO32- |
| B、pH=7的溶液中:Fe3+、K+、SO42-、Br- |
| C、c(H+)/c (OH-)═104的溶液:K+、Ba2+、NO3-、Cl- |
| D、水电离出的c(H+)═1.0×10-13 mol?L-1的溶液中:SO42-、K+、Cl-、Fe3+ |
考点:离子共存问题
专题:离子反应专题
分析:A.使甲基橙变红色的溶液呈强酸性,弱酸根离子等和氢离子反应的离子不能大量存在;
B.常温下,pH=7的溶液呈中性,离子之间不能反应生成气体、沉淀、弱电解质或发生氧化还原反应、双水解反应;
C.c(H+)/c (OH-)═104的溶液呈酸性,离子之间不能反应且和氢离子不能反应;
D.水电离出的c(H+)═1.0×10-13 mol?L-1的溶液呈酸性或碱性,离子之间不能反应且和氢离子或氢氧根离子都不能反应.
B.常温下,pH=7的溶液呈中性,离子之间不能反应生成气体、沉淀、弱电解质或发生氧化还原反应、双水解反应;
C.c(H+)/c (OH-)═104的溶液呈酸性,离子之间不能反应且和氢离子不能反应;
D.水电离出的c(H+)═1.0×10-13 mol?L-1的溶液呈酸性或碱性,离子之间不能反应且和氢离子或氢氧根离子都不能反应.
解答:
解:A.使甲基橙变红色的溶液呈强酸性,碳酸根离子和氢离子反应生成二氧化碳和水,所以不能大量共存,故A错误;
B.常温下,pH=7的溶液呈中性,中性条件下,铁离子和氢氧根离子反应生成氢氧化铁沉淀,故B错误;
C.c(H+)/c (OH-)═104的溶液呈酸性,这几种离子之间不反应且和氢离子也不反应,所以能大量共存,故C正确;
D.水电离出的c(H+)═1.0×10-13 mol?L-1的溶液呈酸性或碱性,碱性条件下,铁离子和氢氧根离子反应而不能大量共存,故D错误;
故选C.
B.常温下,pH=7的溶液呈中性,中性条件下,铁离子和氢氧根离子反应生成氢氧化铁沉淀,故B错误;
C.c(H+)/c (OH-)═104的溶液呈酸性,这几种离子之间不反应且和氢离子也不反应,所以能大量共存,故C正确;
D.水电离出的c(H+)═1.0×10-13 mol?L-1的溶液呈酸性或碱性,碱性条件下,铁离子和氢氧根离子反应而不能大量共存,故D错误;
故选C.
点评:本题考查离子共存,为高考高频点,侧重考查复分解反应,明确复分解反应的条件即可解答,易错选项是B.

练习册系列答案
相关题目
在自然界中,既能以化合态存在又能以游离态存在的元素是( )
| A、碳 | B、硅 | C、氯 | D、铝 |
下列关于能源的说法不正确的是( )
| A、煤的干馏是物理变化,煤的气化和液化是化学变化 |
| B、煤油可由石油分馏获得,可用作燃料和保存少量金属钠 |
| C、沼气(主要成分是CH4)是可再生能源 |
| D、太阳能、氢能、风能、地热能、生物质能都是新能源 |
下列有关金属腐蚀与防护的说法中,不正确的是( )
| A、温度越高,金属腐蚀越快 |
| B、金属被腐蚀的本质是发生了氧化反应 |
| C、将钢闸门与直流电源的正极相连可防止其被腐蚀 |
| D、在铁管上镀锌可防止其被腐蚀 |
下列盐的溶液蒸干时,能得到原物质的是( )
| A、Na2SO3 |
| B、FeCl3 |
| C、KNO3 |
| D、NH4HCO3 |
下列化学用语描述中正确的是( )
A、含18个中子的氯原子的核素符号:
| ||
B、比例模型 可以表示CO2 分子或SiO2分子 可以表示CO2 分子或SiO2分子 | ||
| C、HCO3-的电离方程式为:HCO3-+H2O?CO32-+H3O+ | ||
| D、次氯酸的结构式:H-Cl-O |
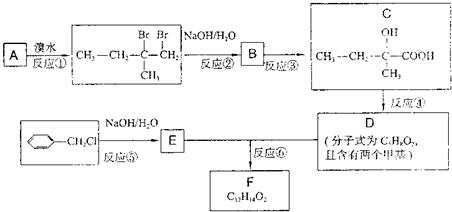
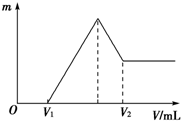 将0.1mol的镁和铝的混合物溶于50mL 4mol?L-1 H2SO4溶液中,然后再滴加2mol?L-1的NaOH溶液.请回答下列问题:
将0.1mol的镁和铝的混合物溶于50mL 4mol?L-1 H2SO4溶液中,然后再滴加2mol?L-1的NaOH溶液.请回答下列问题: