题目内容
25℃时,部分物质的电离平衡常数如表所示:
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为 .
(2)同浓度CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为 .
(3)物质的量浓度均为0.1mol?L-1 的下列四种物质的溶液:a.Na2CO3、b.NaClO、c.CH3COONa、d.NaHCO3,pH由大到小的顺序是 .
(4)常温下0.1 mol?L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是 (填序号).
A.c(H+) B.
C.c(H+)?c(OH-) D.
E.
若该溶液升高温度,上述5种表达式的数据增大的是 .
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(2)同浓度CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为
(3)物质的量浓度均为0.1mol?L-1 的下列四种物质的溶液:a.Na2CO3、b.NaClO、c.CH3COONa、d.NaHCO3,pH由大到小的顺序是
(4)常温下0.1 mol?L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是
A.c(H+) B.
| c(H+) |
| c(CH3COOH) |
| c(OH-) |
| c(H+) |
| c(CH3COO-)?c(H+) |
| c(CH3COOH) |
若该溶液升高温度,上述5种表达式的数据增大的是
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:(1)电离平衡常数越大,酸的电离程度越大,溶液酸性越强;
(2)酸根离子对应酸的酸的电离平衡常数越大,则其结合氢离子能力越弱;
(3)酸根离子对应酸的酸性越强,该离子的水解程度越小,溶液的pH越小;
(4)CH3COOH溶液加水稀释过程中,醋酸的电离程度增大,氢离子浓度、醋酸根离子浓度减小,但氢氧根离子浓度增大;由于温度不变,则电离平衡常数、水的离子积不变;升高温度后醋酸的电离程度增大,则溶液中氢离子浓度增大、水的离子积增大、电离平衡常数增大.
(2)酸根离子对应酸的酸的电离平衡常数越大,则其结合氢离子能力越弱;
(3)酸根离子对应酸的酸性越强,该离子的水解程度越小,溶液的pH越小;
(4)CH3COOH溶液加水稀释过程中,醋酸的电离程度增大,氢离子浓度、醋酸根离子浓度减小,但氢氧根离子浓度增大;由于温度不变,则电离平衡常数、水的离子积不变;升高温度后醋酸的电离程度增大,则溶液中氢离子浓度增大、水的离子积增大、电离平衡常数增大.
解答:
解:(1)根据表中数据可知,酸的电离出平衡常数大小为:CH3COOH>H2CO3>HCO3->HClO,电离平衡常数越大,酸性越强,所以酸性由强到弱的顺序为为:CH3COOH>H2CO3>HClO,
故答案为:CH3COOH>H2CO3>HClO;
(2)酸根离子对应酸的酸的电离平衡常数越大,则其结合氢离子能力越弱,由于电离平衡常数CH3COOH>H2CO3>HCO3->HClO,则同浓度CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为:CO32->ClO->HCO3->CH3COO-,
故答案为:CO32->ClO->HCO3->CH3COO-;
(3)四种溶液的溶质都是强碱弱酸盐,水解程度大小为:CO32->ClO->HCO3->CH3COO-,水解均显碱性,水解程度越大,碱性越强,所以碱性顺序是:Na2CO3>NaClO>NaHCO3>CH3COONa,
即pH由小到大的排列顺序为:CH3COONa<NaHCO3<NaClO<Na2CO3,即:pH由大到小的顺序为:abdc,
故答案为:abdc;
(4)A、0.1mol?L-1的CH3COOH溶液加稀释过程中,溶液中氢离子浓度减小,故A正确;
B、0.1mol?L-1的CH3COOH溶液加稀释过程中,各个微粒浓度减小,同时醋酸的电离向右移动,c(H+)减小的程度小于c(CH3COOH)的减小程度,所以
增大,故B错误;
C、Kw=c(H+)?c(OH-)只受温度的影响,温度不变则其值是一个常数,故C错误;
D、醋酸稀释,酸性减弱,c(H+)减小,水的离子积不变,则c(OH-)增大,所以
增大,故D错误;
E、
为醋酸的电离平衡常数,由于温度不变,则水的电离平衡常数不变,故E错误;
故答案为:A;
若该溶液升高温度,醋酸、水的电离程度对增大,则溶液中氢离子、氢氧根离子浓度都增大,
A.升高温度后溶液中氢离子浓度c(H+)增大,故A正确;
B.升高温度后氢离子、氢氧根离子浓度都增大,
,醋酸的浓度减小,则该比值增大,故B正确;
C.c(H+)?c(OH-)为水的离子积,升高温度后水的电离程度增大,则水的离子积增大,故C正确;
D.
,升高温度后氢氧根离子、氢离子浓度都增大,但氢氧根离子浓度增大的幅度大于氢氧根离子,所以该比值减小,故D错误;
E.
为醋酸的电离平衡常数,升高温度后产生的电离平衡常数增大,故E正确;
故答案为:ABCE.
故答案为:CH3COOH>H2CO3>HClO;
(2)酸根离子对应酸的酸的电离平衡常数越大,则其结合氢离子能力越弱,由于电离平衡常数CH3COOH>H2CO3>HCO3->HClO,则同浓度CH3COO-、HCO3-、CO32-、ClO-结合H+的能力由强到弱的顺序为:CO32->ClO->HCO3->CH3COO-,
故答案为:CO32->ClO->HCO3->CH3COO-;
(3)四种溶液的溶质都是强碱弱酸盐,水解程度大小为:CO32->ClO->HCO3->CH3COO-,水解均显碱性,水解程度越大,碱性越强,所以碱性顺序是:Na2CO3>NaClO>NaHCO3>CH3COONa,
即pH由小到大的排列顺序为:CH3COONa<NaHCO3<NaClO<Na2CO3,即:pH由大到小的顺序为:abdc,
故答案为:abdc;
(4)A、0.1mol?L-1的CH3COOH溶液加稀释过程中,溶液中氢离子浓度减小,故A正确;
B、0.1mol?L-1的CH3COOH溶液加稀释过程中,各个微粒浓度减小,同时醋酸的电离向右移动,c(H+)减小的程度小于c(CH3COOH)的减小程度,所以
| c(H+) |
| c(CH3COOH) |
C、Kw=c(H+)?c(OH-)只受温度的影响,温度不变则其值是一个常数,故C错误;
D、醋酸稀释,酸性减弱,c(H+)减小,水的离子积不变,则c(OH-)增大,所以
| c(OH-) |
| c(H+) |
E、
| c(CH3COO-)?c(H+) |
| c(CH3COOH) |
故答案为:A;
若该溶液升高温度,醋酸、水的电离程度对增大,则溶液中氢离子、氢氧根离子浓度都增大,
A.升高温度后溶液中氢离子浓度c(H+)增大,故A正确;
B.升高温度后氢离子、氢氧根离子浓度都增大,
| c(H+) |
| c(CH3COOH) |
C.c(H+)?c(OH-)为水的离子积,升高温度后水的电离程度增大,则水的离子积增大,故C正确;
D.
| c(OH-) |
| c(H+) |
E.
| c(CH3COO-)?c(H+) |
| c(CH3COOH) |
故答案为:ABCE.
点评:本题考查了弱电解质的电离及其影响,题目难度中等,试题知识点较多、综合性较强,充分考查了学生的分析、理解能力及灵活应用所学知识的能力,明确温度、浓度等对电离平衡常数、水的离子积的影响为解答关键.

练习册系列答案
相关题目
工业上制造金刚砂(SiC)的化学反应如下:SiO2+3C═SiC+2CO↑,在这个反应中,氧化剂和还原剂的物质的量之比是( )
| A、1:2 | B、2:1 |
| C、1:1 | D、3:1 |
对于反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,下列说法正确的是( )
| A、只有硫酸铜作氧化剂 |
| B、SO42-既不是氧化产物又不是还原产物 |
| C、被氧化与被还原的硫元素的质量比为3:7 |
| D、当有1mol硫酸铜参加反应时,该反应转移1mol电子 |
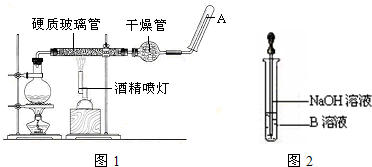
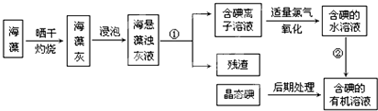
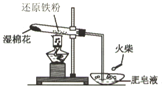 为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验.
为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验.