题目内容
小明很喜欢化学实验课,今天要学习“探究铁及其化合物的氧化性或还原性”,现邀你一起走进他的化学课堂.
(1)课前老师布置了下列预习作业,请你一起完成:
①铁不同价态的物质各写一种(并标出铁元素的化合价): 、 、
②写出一个他们之间相互转化(含三种价态)的化学方程式:
(2)实验室提供的下列试剂:锌粒、铁粉、0.1mol?L -1 FeCl 3 溶液、0.1mol?L -1 FeCl 2 溶液、KSCN 溶液、新制氯水,探究 Fe 2+、Fe 3+ 的氧化性、还原性.
根据氧化还原的有关原理,小明说 Fe 2+ 既有还原性又有氧化性; 为证实自己的假设,请你和小明一起设计实验方案,进行实验并描述实验现象,完成下列表格.
(3)小明家有一瓶近无色的补血剂,请你设计一个实验方案,检验其中铁元素的价态. .
(1)课前老师布置了下列预习作业,请你一起完成:
①铁不同价态的物质各写一种(并标出铁元素的化合价):
②写出一个他们之间相互转化(含三种价态)的化学方程式:
(2)实验室提供的下列试剂:锌粒、铁粉、0.1mol?L -1 FeCl 3 溶液、0.1mol?L -1 FeCl 2 溶液、KSCN 溶液、新制氯水,探究 Fe 2+、Fe 3+ 的氧化性、还原性.
根据氧化还原的有关原理,小明说 Fe 2+ 既有还原性又有氧化性; 为证实自己的假设,请你和小明一起设计实验方案,进行实验并描述实验现象,完成下列表格.
| 探究内容 | 实验方案 | 实验现象 |
| 探究 Fe 2+ 具有还原性 | ||
| 探究 Fe 2+ 具有氧化性 |
考点:性质实验方案的设计
专题:实验设计题
分析:(1)①根据铁有的化合价0、+2、+3价来书写;
②根据铁归中反应书写;
(2)亚铁离子中的铁是+2价,居于铁元素的中间价态,具有还原性和氧化性,当遇到强还原剂时显示氧化性,对应还原产物金属单质铁,当遇到氧化剂时,表现还原性,对应氧化产物是三价铁,亚铁离子浅绿色,三价铁离子是棕黄色;
(3)根据检验三价铁的方法来检验.
②根据铁归中反应书写;
(2)亚铁离子中的铁是+2价,居于铁元素的中间价态,具有还原性和氧化性,当遇到强还原剂时显示氧化性,对应还原产物金属单质铁,当遇到氧化剂时,表现还原性,对应氧化产物是三价铁,亚铁离子浅绿色,三价铁离子是棕黄色;
(3)根据检验三价铁的方法来检验.
解答:
解:(1)①铁有的化合价0、+2、+3价,0价的为Fe,+2价的为FeCl2,+3价的为FeCl3,故答案为:Fe;FeCl2;FeCl3;
②Fe,FeCl2,FeCl3相互转化的方程式为:Fe+2FeCl3═3FeCl2,故答案为:Fe+2FeCl3═3FeCl2;
(2)亚铁离子中的铁是+2价,当遇到强还原剂金属锌时,显示氧化性,发生置换反应:Zn+Fe2+=Zn2++Fe,对应还原产物金属单质铁,该反应证明Fe2+具有氧化性;
在FeCl2溶液中加入适量氧化剂氯水,亚铁离子会从+2价升高到+3价,溶液由浅绿色变为棕黄色,再加入KSCN溶液又会变成血红色,即2Fe2++Cl2=2Fe3++2Cl-,体现了亚铁离子的还原性,故答案为:
(3)检验其中铁元素的价态为:取少量药液,加水稀释后加入KSCN溶液,若溶液变血红色,说明药液中含Fe3+,不变血红色,则含二价铁,
故答案为:取少量药液,加水稀释后加入KSCN溶液,若溶液变血红色,说明药液中含Fe3+,不变血红色,则含二价铁.
②Fe,FeCl2,FeCl3相互转化的方程式为:Fe+2FeCl3═3FeCl2,故答案为:Fe+2FeCl3═3FeCl2;
(2)亚铁离子中的铁是+2价,当遇到强还原剂金属锌时,显示氧化性,发生置换反应:Zn+Fe2+=Zn2++Fe,对应还原产物金属单质铁,该反应证明Fe2+具有氧化性;
在FeCl2溶液中加入适量氧化剂氯水,亚铁离子会从+2价升高到+3价,溶液由浅绿色变为棕黄色,再加入KSCN溶液又会变成血红色,即2Fe2++Cl2=2Fe3++2Cl-,体现了亚铁离子的还原性,故答案为:
| 实验方案 | 实验现象 |
| 在FeCl2溶液中加入适量氯水,再加入少量的KSCN溶液 | 加入适量氯水,溶液由浅绿色变为棕黄色,再加入少量的KSCN溶液,溶液变成血红色 |
| 在FeCl2溶液中加入锌片 | 溶液由浅绿色变为无色,锌片表面有黑色物质产生 |
故答案为:取少量药液,加水稀释后加入KSCN溶液,若溶液变血红色,说明药液中含Fe3+,不变血红色,则含二价铁.
点评:本题考查学生铁以及化合物之间的性质,是一道涉及氧化还原反应知识的实验探究题目,难度不是很大.

练习册系列答案
相关题目
在标准状况下,m g气体A与n g气体B的分子数相同,下列说法中不正确的是( )
| A、两种气体A与B的相对分子质量之比为m:n |
| B、同质量气体A与B的分子数之比为m:n |
| C、同温同压下,A、B两气体的密度之比为n:m |
| D、相同状况下,同体积A、B两气体的质量之比为m:n |
按照下列分类方式可以将NaHCO3和KHSO4归为一类的是( )
| A、强碱 | B、酸式盐 | C、氧化物 | D、酸 |
下列离子方程式与所述事实相符且正确的是( )
| A、用H2O2酸性溶液,将海带灰中的I-转变为I2:H2O2+2I-═I2+2OH- |
| B、高锰酸钾与足量浓盐酸反应制氯气:2MnO4-+16H++10Cl-═2Mn2++5Cl2↑+8H2O |
| C、AlCl3溶液中滴加过量氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
| D、漂白粉溶液中,通入过量的二氧化碳:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO |
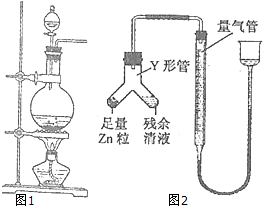 实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图1示).
实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图1示).