题目内容
15.常温下,浓度为0.05mol•L-1的H2SO4溶液其PH值为( )| A. | 2 | B. | 13 | C. | 1 | D. | 1.3 |
分析 先计算出该硫酸溶液中氢离子浓度,然后根据pH=-lgc(H+)计算出该硫酸溶液的pH.
解答 解:0.05mol•L-1的H2SO4溶液中氢离子浓度为:c(H+)=0.05mol/L×2=0.1mol,
该硫酸溶液的pH=-lgc(H+)=-lg0.1=1,
故选C.
点评 本题考查了溶液pH的简单计算,题目难度不大,明确pH的概念及表达式为解答关键,试题侧重基础知识的考查,培养了学生的化学计算能力.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
9.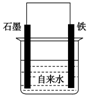 为探究钢铁的吸氧腐蚀原理设计了如图所示装置,下列有关说法中错误的是( )
为探究钢铁的吸氧腐蚀原理设计了如图所示装置,下列有关说法中错误的是( )
 为探究钢铁的吸氧腐蚀原理设计了如图所示装置,下列有关说法中错误的是( )
为探究钢铁的吸氧腐蚀原理设计了如图所示装置,下列有关说法中错误的是( )| A. | 正极的电极方程式为:O2+2H2O+4e-═4OH- | |
| B. | 将石墨电极改成Mg电极,难以观察到铁锈生成 | |
| C. | 若向自来水中加入少量NaCl(s),可较快地看到铁锈 | |
| D. | 断开连接石墨和铁的导线,铁便不会生锈 |
3.类比是化学学习中常用的方法,已知硝酸能把铁氧化成Fe(NO3)3,但当铁过量时,产物是Fe(NO3)2.某同学受此启发,提出一个相似的观点:氯气与铁粉反应,当Cl2足量时生成FeCl3,当铁粉过量时是FeCl2,为验证该观点是否正确,该同学将一定量铁粉与Cl2恰好完全反应得到一固体物质,然后通过实验确定其成分.探究过程如下:请填空:
(1)提出假设:
假设1:该固体物质是FeCl2
假设2:该固体物质是FeCl3
假设3:该固体物质是FeCl3和FeCl2的混合物
(2)设计方案:
取少量固体物质于烧杯中,加适量水溶解,得到溶液A,然后取两份A溶液分别进行实验,实验现象与结论如下表,请将表中现象和结论补充完整.
(3)根据上述实验结论,写出Cl2与铁粉加热时发生反应的化学方程式2Fe+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3.
(4)为进一步探究FeCl3溶液的性质,他又利用A溶液做了如下一些实验,其中明显错误的一项是D
A.将A溶液滴入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔现象
B.铜片放入在A溶液中,铜片会被溶蚀
C.在A溶液中滴加NaOH浓溶液,出现红褐色沉淀
D.在A溶液中加入碘化钾淀粉溶液无明显现象.
(1)提出假设:
假设1:该固体物质是FeCl2
假设2:该固体物质是FeCl3
假设3:该固体物质是FeCl3和FeCl2的混合物
(2)设计方案:
取少量固体物质于烧杯中,加适量水溶解,得到溶液A,然后取两份A溶液分别进行实验,实验现象与结论如下表,请将表中现象和结论补充完整.
| 实验方法 | 实验现象 | 结 论 |
| 在溶液中加KSCN溶液 | 溶液变红色 | 固体物质中有FeCl3 |
| 在KMnO4溶液中加少量A溶液 | KMnO4溶液颜色无明显变化 | 固体物质中不含FeCl2 |
(4)为进一步探究FeCl3溶液的性质,他又利用A溶液做了如下一些实验,其中明显错误的一项是D
A.将A溶液滴入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔现象
B.铜片放入在A溶液中,铜片会被溶蚀
C.在A溶液中滴加NaOH浓溶液,出现红褐色沉淀
D.在A溶液中加入碘化钾淀粉溶液无明显现象.
10.下列反应的离子方程式中,正确的是( )
| A. | 稀硫酸滴在银片上:2Ag+2H+═2Ag++H2↑ | |
| B. | 碳酸钠与稀盐酸的反应:CO32-+2H+═H2O+CO2↑ | |
| C. | Mg(OH)2与盐酸的反应:H++OH-═H2O | |
| D. | 铜片放入ZnSO4溶液中:Cu+Zn2+═Cu2++Zn |
20.常温下将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表:
下列对混合后溶液的有关说法中,不正确的是( )
| 实验编号 | c(HA)/mol•L-1 | c(NaOH)/mol•L-1 | 混合后溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | b | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH<7 |
| 丁 | 0.1 | 0.1 | pH=c |
| A. | 甲中:若a=7,则HA是强酸 | |
| B. | 乙中:若b≠0.2,则c(A-)≠c(Na+) | |
| C. | 丙中:若HA是弱酸,则c(A-)>c(Na+)>c(H+)>c(OH-) | |
| D. | 丁中:若c=9,则c(OH-)-c(HA)=10-9mol•L-1 |
5.电子表和电子计算器的电源常用微型银锌原电池,其电极分别为Ag2O和Zn,电解质溶液为KOH溶液,放电时锌极上的电极反应式为:Zn+2OH--2e-═Zn(OH)2;氧化银电极上的反应式为:Ag2O+H2O+2e-═2Ag+2OH-,总反应式为:Ag2O+H2O+Zn═Zn(OH)2+2Ag.下列说法正确的是( )
| A. | 锌是负极,发生氧化反应 | |
| B. | 锌的质量减少6.5g,外电路中通过0.4mol电子 | |
| C. | 溶液中OH-向正极移动,K+、H+向负极移动 | |
| D. | 随着电极反应的不断进行,电解质溶液中n(OH-)减小 |