题目内容
图中①~⑩分别代表有关反应中的一种物质,它们均为中学化学中的常见物质.已知①~⑤和⑥~⑩中分别含有同一种元素.反应⑤→①+O2的条件未标出,请填写以下空白.

(1)①、⑥的化学式分别是 , .
(2)②与③反应的离子方程式是
(3)⑨→⑩的化学方程式是 .

(1)①、⑥的化学式分别是
(2)②与③反应的离子方程式是
(3)⑨→⑩的化学方程式是
考点:无机物的推断,常见金属元素的单质及其化合物的综合应用
专题:推断题
分析:①能和酸反应也能和碱反应,说明①为Al或氧化铝或氢氧化铝,故①~⑤都含有Al元素,⑤反应得到氧气与①,应是电解氧化铝得到氧气与铝,故①为Al、⑤为Al2O3,②是铝盐、③是偏铝酸盐,④为Al(OH)3.铝和⑥能在高温下发生反应生成⑦和氧化铝,则该反应为铝热反应,⑥为金属氧化物,⑦是金属单质,⑦和酸反应生成⑧,⑧和氢氧根离子反应生成氢氧化物⑨,⑨能被氧气氧化生成⑩,⑩分解生成⑥,能被空气中被氧化的氢氧化物是Fe(OH)2,则⑨是Fe(OH)2,⑩是Fe(OH)3,⑥是Fe2O3,⑦是Fe,⑧为亚铁盐,据此解答.
解答:
解:①能和酸反应也能和碱反应,说明①为Al或氧化铝或氢氧化铝,故①~⑤都含有Al元素,⑤反应得到氧气与①,应是电解氧化铝得到氧气与铝,故①为Al、⑤为Al2O3,②是铝盐、③是偏铝酸盐,④为Al(OH)3.铝和⑥能在高温下发生反应生成⑦和氧化铝,则该反应为铝热反应,⑥为金属氧化物,⑦是金属单质,⑦和酸反应生成⑧,⑧和氢氧根离子反应生成氢氧化物⑨,⑨能被氧气氧化生成⑩,⑩分解生成⑥,能被空气中被氧化的氢氧化物是Fe(OH)2,则⑨是Fe(OH)2,⑩是Fe(OH)3,⑥是Fe2O3,⑦是Fe,⑧为亚铁盐,
(1)由上述分析可知,①、⑥的化学式分别是:Al,Fe2O3,故答案为:Al;Fe2O3;
(2)②与③是铝盐和偏铝酸盐反应生成氢氧化铝,离子反应方程式为:Al3++3AlO2-+6H2O=4Al(OH)3↓,
故答案为:Al3++3AlO2-+6H2O=4Al(OH)3↓;
(3)⑨→⑩是氢氧化亚铁被空气氧化生成氢氧化铁,反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 ,
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 .
(1)由上述分析可知,①、⑥的化学式分别是:Al,Fe2O3,故答案为:Al;Fe2O3;
(2)②与③是铝盐和偏铝酸盐反应生成氢氧化铝,离子反应方程式为:Al3++3AlO2-+6H2O=4Al(OH)3↓,
故答案为:Al3++3AlO2-+6H2O=4Al(OH)3↓;
(3)⑨→⑩是氢氧化亚铁被空气氧化生成氢氧化铁,反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 ,
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 .
点评:本题考查无机物推断,“铝的两性及铝热反应”为突破口,采用正逆相结合的方法进行推断,明确物质的性质及物质之间的转化是解本题关键,难度中等.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
有X、Y、Z、W、M五种原子序数依次增大的短周期主族元素,其中X元素的气态氢化物水溶液显碱性,离子半径Y2->W3+,Y、Z元素的最外层电子数之和等于M元素的最外层电子数.下列说法正确的是( )
| A、X、Y形成的气态氢化物的沸点前者高 |
| B、W、M形成的化合物可作为水处理中的消毒剂 |
| C、工业上通常用电解法制备Z、W、M的单质 |
| D、X、Z形成的化合物ZX3和Z3X所含键的类型相同 |
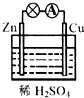 在如图所示的原电池中,正极发生的反应是( )
在如图所示的原电池中,正极发生的反应是( )| A、2H++2e-═H2↑ |
| B、Cu-2e-═Cu2+ |
| C、Cu2++2e-═Cu |
| D、Zn-2e-═Zn2+ |
若49g H2SO4含有的O原子数为N,则阿佛加德罗常数(NA)等于( )
A、
| ||
B、
| ||
| C、N个 | ||
| D、2N L/mol |
下列事实不能用化学平衡移动原理解释的是( )
| A、在强碱存在的条件下,酯在水中的溶解度增大 |
| B、加催化剂,使氮气和氢气在一定条件下转化为氨气 |
| C、可用浓氨水和氢氧化钠固体快速制取氨气 |
| D、500℃左右比室温更有利于合成氨反应 |

