题目内容
对于可逆反应2A2(g)+B2(g)?2A2B(l)(正反应为放热反应)达到平衡,要使正、逆反应的速率都增大,而且平衡向右移动,可以采取的措施是( )
| A、升高温度 | B、降低温度 |
| C、增大压强 | D、减小压强 |
考点:化学平衡的影响因素
专题:电离平衡与溶液的pH专题
分析:达平衡时,要使正、逆反应的速率都增大,可采取升高温度、增大压强或增大浓度的措施,使平衡向正反应方向移动,依据反应特征结合化学平衡移动原理分析,降温增大压强平衡正向进行;综合两种变化选择采取的措施.
解答:
解:A、反应是放热反应,升温,反应速率增大,正逆反应速率增大,平衡逆向进行,故A不符合;
B、降低温度正逆反应速率减小,平衡正向进行,故B不符合;
C、反应是气体体积减小的反应增大压强,反应速率增大,平衡正向进行,故C符合;
D、减小压强反应速率减小,平衡逆向进行,故D不符合;
故选C.
B、降低温度正逆反应速率减小,平衡正向进行,故B不符合;
C、反应是气体体积减小的反应增大压强,反应速率增大,平衡正向进行,故C符合;
D、减小压强反应速率减小,平衡逆向进行,故D不符合;
故选C.
点评:本题考查了化学平衡移动原理的分析判断,反应速率影响因素理解应用,掌握平衡移动原理和反应特征是解题关键,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
常温下,在溶液中可发生以下反应:①16H++10Z-+2XO4-═2X2++5Z2+8H2O,②2M2++R2═2M3++2R-,③2R-+Z2═R2+2Z-,由此判断下列说法错误的是( )
| A、常温下反应2M2++Z2═2M3++2Z-可以自发进行 |
| B、Z元素在反应①中被氧化,在③中被还原 |
| C、氧化性强弱顺序为:XO4-<Z2<R2<M3+ |
| D、还原性强弱顺序为:X2+<Z-<R-<M2+ |
下列属于离子反应的是( )
| A、H2和O2反应生成水 |
| B、将浓硫酸稀释 |
| C、KClO3和MnO2混合共热制O2 |
| D、CuSO4溶液中加入NaOH溶液 |
关于Li、Na、K、Rb、Cs的叙述均正确的一组是( )
①金属性最强的是铯
②氧化性最强的是锂原子
③在自然界中均以化合态形式存在
④密度按Li-Cs 顺序呈依次递增趋势
⑤铯与水反应十分剧烈,甚至会发生爆炸
⑥它们的 氧化物都只有M20和M202两种形式
⑦粒子半径:Rb+>K+>Na+,Cs>Cs+>K+,K>Na>Li.
①金属性最强的是铯
②氧化性最强的是锂原子
③在自然界中均以化合态形式存在
④密度按Li-Cs 顺序呈依次递增趋势
⑤铯与水反应十分剧烈,甚至会发生爆炸
⑥它们的 氧化物都只有M20和M202两种形式
⑦粒子半径:Rb+>K+>Na+,Cs>Cs+>K+,K>Na>Li.
| A、①②③④ | B、④⑤⑥⑦ |
| C、②⑥ | D、①③⑤⑦ |
下列说法正确的是( )
| A、强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 |
| B、固体硫酸钠不能导电,所以它不是电解质 |
| C、铜丝能够导电,所以铜丝是电解质 |
| D、二氧化碳溶于水形成的溶液可以导电,但二氧化碳是非电解质 |
下列各组物质之间是同系物的是( )
| A、CH3CH2COOH与CH3COOCH3 |
B、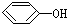 与 与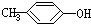 |
| C、2、2-二甲基丙烷与2-甲基丁烷 |
D、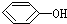 与 与 |
下列变化属于化学变化的是( )
| A、路面的水结成冰 |
| B、地震中房屋的倒塌 |
| C、电解水得到氢气和氧气 |
| D、将铁丝弯成奥运五环 |
KCl中含有的化学键是( )
| A、离子键 | B、极性键 |
| C、非极性键 | D、共价键 |
 试回答下列问题:
试回答下列问题: