题目内容
5.(1)写出NaHCO3在水中电离的方程式NaHCO3=Na++HCO3-,其水溶液显碱性的原因用离子方程式表示为HCO3-+H2O?H2CO3+OH-.(2)金属Mg放入NH4Cl溶液中产生H2的过程用离子方程式表示为Mg+2NH4++2H2O=2NH3•H2O+Mg2++H2↑.
分析 (1)碳酸氢钠为强电解质,在溶液中完全电离出钠离子和碳酸氢根离子;碳酸氢根离子水解生成碳酸和企业广告离子,溶液呈碱性;
(2)氯化铵溶液中,铵根离子水解导致溶液显示酸性,则金属Mg放入NH4Cl溶液中产生H2.
解答 解:(1)NaHCO3在水中完全电离,其电离的方程式为:NaHCO3=Na++HCO3-;由于碳酸氢根离子在溶液中存在水解反应:HCO3-+H2O?H2CO3+OH-,导致溶液呈碱性,
故答案为:NaHCO3=Na++HCO3-;HCO3-+H2O?H2CO3+OH-;
(2)氯化铵溶液中,铵根离子水解溶液呈酸性,金属Mg与氢离子反应生成氢气,反应的离子方程式为:Mg+2NH4++2H2O=2NH3•H2O+Mg2++H2↑,
故答案为:Mg+2NH4++2H2O=2NH3•H2O+Mg2++H2↑.
点评 本题考查离子方程式、电离方程式的书写,为高考的高频题,题目难度不大,明确发生反应原理为解答关键,注意掌握离子方程式、电离方程式的书写原则,试题侧重基础知识的考查,有利于提高学生的灵活应用能力.

练习册系列答案
相关题目
13.下列物质属于糖类的是( )
| A. | 蛋白质 | B. | 花生油 | C. | 柠檬黄 | D. | 纤维素 |
20.已知4NH3+5O2=4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系是( )
| A. | v(NH3)=$\frac{2}{3}$v(H2O) | B. | v(O2)=$\frac{6}{5}$v(H2O) | C. | v(NH3)=$\frac{5}{4}$v(O2) | D. | v(O2)=$\frac{4}{5}$v(NO) |
10.在氯水中存在多种分子和离子,它们在不同的反应中表现各自的性质.下列实验现象和结论不一致的是( )
| A. | 加入有色布条,一会儿有色布条褪色,说明溶液中有HC1O存在 | |
| B. | 溶液呈黄绿色,且有刺激性气味,说明有C12分子存在 | |
| C. | 加入硝酸酸化的AgNO3溶液产生白色沉淀,说明有C1-存在 | |
| D. | 加入NaOH溶液,氯水黄绿色消失,说明有HC1O分子存在 |
14.列有关说法正确的是( )
| A. | 江河入海口三角洲的形成通常与胶体的性质有关 | |
| B. | 活泼金属元素的氧化物一定是碱性氧化物,非金属元素的氧化物一定是酸性氧化物 | |
| C. | H+、K+、S2-、Br-能在Fe(OH)3胶体中大量共存 | |
| D. | AgI胶体在电场中定向运动,是因为胶体是带电的 |
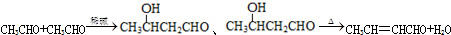
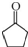
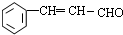 +2Cu(OH)2 $\stackrel{△}{→}$
+2Cu(OH)2 $\stackrel{△}{→}$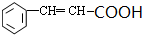 +Cu2O↓+3H2O.
+Cu2O↓+3H2O.