题目内容
5.现有4g氢氧化钠恰好与100ml的盐酸完全反应,试计算(写计算过程)(1)氢氧化钠的物质的量
(2)钠离子的数目.
分析 发生NaOH+HCl=NaCl+H2O,n(NaOH)=$\frac{4g}{40g/mol}$=0.1mol,结合反应计算.
解答 解:(1)n(NaOH)=$\frac{4g}{40g/mol}$=0.1mol,答:氢氧化钠的物质的量为0.1mol;
(2)反应前后钠离子数目不变,n(Na+)=n(NaOH)=n(NaCl)=0.1mol,N=0.1mol×NA=0.1NA个,答:钠离子数目为0.1NA个.
点评 本题考查化学反应的计算,为高频考点,把握发生的反应或物质的量的计算为解答的关键,侧重分析与计算能力的考查,注意基本计算公式的应用,题目难度不大.

练习册系列答案
相关题目
2.下列说法错误的是( )
| A. | 液氨汽化时要吸收大量的热,常用作制冷剂 | |
| B. | 加快清洁能源发展、加强污染物达标排放检查是治理雾霾的有效措施 | |
| C. | 为使水果保鲜,可在水果箱内放入高锰酸钾溶液浸泡过的硅藻土 | |
| D. | 氢氧化铝、碳酸钠都是常见的胃酸中和剂 |
3.化学在生活中有着广泛的应用,下列对应关系错误的是( )
| 化学性质 | 实际应用 | |
| A | Al2(SO4)3和小苏打反应 | 泡沫灭火器灭火 |
| B | 次氯酸盐具有氧化性 | 漂白粉漂白织物 |
| C | HF与SiO2反应 | 氢氟酸在玻璃器皿上刻蚀标记 |
| D | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
| A. | A | B. | B | C. | C | D. | D |
10.如图是实验室制备氯气并验证氯气性质的装置(其中夹持装置已省略)
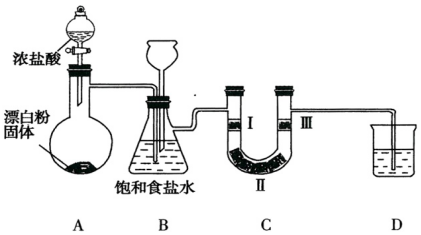
已知:装置A是氯气的发生装置,反应的化学方程式为:
Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.
据此回答下列问题:
(1)装置B中饱和食盐水的作用是除去Cl2中的HCl.
(2)装置B也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:B中长颈漏斗中液面上升.
(3)装置C的目的是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是d(填序号).
(4)装置D的作用是吸收多余的氯气,防止污染空气,则烧杯中的溶液是NaOH溶液,写出所发生反应的化学方程式:Cl2+2NaOH=NaCl+NaClO+H2O.
(5)若所用浓盐酸的浓度为10mol/L,求产生2.24L(标准状况)Cl2时,发生反应的盐酸为40mL.

已知:装置A是氯气的发生装置,反应的化学方程式为:
Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.
据此回答下列问题:
(1)装置B中饱和食盐水的作用是除去Cl2中的HCl.
(2)装置B也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:B中长颈漏斗中液面上升.
(3)装置C的目的是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是d(填序号).
| 编号 | I | II | III |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(5)若所用浓盐酸的浓度为10mol/L,求产生2.24L(标准状况)Cl2时,发生反应的盐酸为40mL.
15.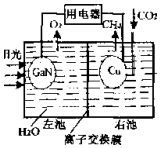 太阳能光电池由于具有可靠性好、寿命长等特点,适于很多特蛛环境和场合,现已得到广泛应用.氮化镓(GaN)光电池的结构如图所示.下列说法中正确的是( )
太阳能光电池由于具有可靠性好、寿命长等特点,适于很多特蛛环境和场合,现已得到广泛应用.氮化镓(GaN)光电池的结构如图所示.下列说法中正确的是( )
 太阳能光电池由于具有可靠性好、寿命长等特点,适于很多特蛛环境和场合,现已得到广泛应用.氮化镓(GaN)光电池的结构如图所示.下列说法中正确的是( )
太阳能光电池由于具有可靠性好、寿命长等特点,适于很多特蛛环境和场合,现已得到广泛应用.氮化镓(GaN)光电池的结构如图所示.下列说法中正确的是( )| A. | 该装置系统中只存在两种能量转化 | |
| B. | Cu电极上的电极反应为:CO2+8e-+8H+═CH4+2H2O | |
| C. | 离子交换膜为质子交换膜,H+从右池移向左池 | |
| D. | 常温下,当装置中有1mol CH4生成时,GaN电极有 44.8LO2生成(不考虑O2的溶解性) |