题目内容
3.如图R、W、X、Y、Z为五种物质,若箭头表示能一步转化的常见反应,则其中常温下能实现图示转化关系的是( )| 选项 | R | W | X | Y | Z |  |
| A | Si | SiO2 | H2SiO3 | Na2SiO3 | SiCl4 | |
| B | Na | Na2O | Na2O2 | Na2CO3 | NaOH | |
| C | Fe | Fe(OH)2 | FeCl2 | FeCl3 | Fe(NO3)3 | |
| D | Al | NaAlO2 | Al2(SO4)3 | AlCl3 | Al(NO3)3 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Si燃烧生成二氧化硅,且Si在常温下不能转化为SiCl4;
B.Na燃烧生成Na2O2;
C.Fe燃烧生成FeCl3,且Fe在常温下不能直接生成Fe(OH)2;
D.Al与硫酸反应生成X,Al与NaOH反应生成W,Al与盐酸反应生成Y,Al与硝酸反应生成Z,X与氯化钡反应生成Y,W与硫酸反应生成X,Y与硝酸银反应生成Z,Z与NaOH生成W.
解答 解:A.Si燃烧生成二氧化硅,且Si在常温下不能转化为SiCl4,Si也不能一步转化为H2SiO3,则常温下不能发生图中转化,故A不选;
B.Na燃烧生成Na2O2,Na在常温下反应生成Na2O,则常温下不能发生图中转化,故B不选;
C.Fe燃烧生成FeCl3,且Fe在常温下不能直接生成Fe(OH)2,则常温下不能发生图中转化,故C不选;
D.Al与硫酸反应生成Al2(SO4)3(X),Al与NaOH反应生成NaAlO2(W),Al与盐酸反应生成AlCl3(Y),Al与硝酸反应生成Al(NO3)3(Z),X与氯化钡反应生成Y,W与硫酸反应生成X,Y与硝酸银反应生成Z,Z与NaOH生成W,反应均可在常温下进行,故D选;
故选D.
点评 本题考查物质的性质及相互转化,综合考查元素化合物知识,把握发生的化学反应及反应条件为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列关于硫酸铜溶液的说法中,不正确的是( )
| A. | 硫酸铜水解使溶液呈酸性 | |
| B. | 升温可促进硫酸铜的水解 | |
| C. | 滴入几滴浓硫酸,硫酸铜的水解程度减小 | |
| D. | 加入少量的硫酸氢钠固体,不影响硫酸铜的水解 |
18.一化学研究性学习小组对某Na2CO3和NaHCO3的混合溶液的组成进行探究,取20.0mL该混合溶液,向其中不断加入1.00mol•L-1的稀盐酸,加入稀盐酸的体积和产生的现象如表中所示.
则混合溶液中c(HCO3-)为( )
| 反应阶段 | Ⅰ | Ⅱ | Ⅲ |
| 稀盐酸体积x/mL | 0<x≤10.0 | 10.0<x≤40.0 | x>40.0 |
| 现 象 | 无气体 | 有气体 | 无气体 |
| A. | 1.00mol•L-1 | B. | 0.50mol•L-1 | C. | 1.50mol•L-1 | D. | 2.00mol•L-1 |
8.下列粒子结构示意图中,表示阳离子的是( )
| A. |  | B. |  | C. |  | D. |  |
12.某温度下,在容积不变的密闭容器中,反应2A(g)+B(g)?2C(g)达到平衡时,A、B、C的物质的量分别为4mol、2mol和4mol,保持温度和容积不变,对平衡混合物中三者的物质的量做如下调整,A的转化率降低的是( )
| A. | 均加倍 | B. | 加入1mol C | C. | 均增加1mol | D. | 均减半 |
 ,其一氯代物的结构简式是
,其一氯代物的结构简式是 ;其中一氯代物种类最多的是
;其中一氯代物种类最多的是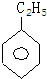 .(均填结构简式)
.(均填结构简式)