题目内容
已知:HCN(aq)与NaOH(aq)反应的ΔH=-12.1 kJ·mol-1;HCl(aq)与NaOH(aq)反应的ΔH=-57.3 kJ·mol-1,则HCN在水溶液中电离的ΔH等于 ( )。
A.-69.4 kJ·mol-1 B.-45.2 kJ·mol-1
C.+45.2 kJ·mol-1 D.+69.4 kJ·mol-1
C
【解析】 根据盖斯定律,将HCN与NaOH的反应设计为以下两步:
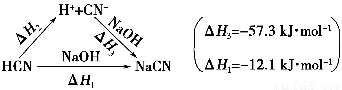
则ΔH1=ΔH2+ΔH3即-12.1 kJ·mol-1
=ΔH2+(-57.3 kJ·mol-1) ΔH2=+45.2 kJ·mol-1。

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案某研究小组在实验室中用铜粉(含铁粉5%以上)制取胆矾(CuSO4·5H2O)并检验其纯度,限选试剂:3 mol·L-1H2SO4溶液、浓硝酸、3%H2O2溶液、0.2 mol·L-1NaOH溶液、20% KSCN溶液、BaCl2溶液。有关物质溶解度如下表(单位g/100 g H2O):
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
CuSO4 | 14.3 | 20.7 | 28.5 | 40.0 | 55.0 | 75.4 |
Cu(NO3)2 | 81.8 | 124.8 | 163.1 | 181.8 | 207.8 | 247.3 |
(1)完成制取胆矾的实验方案。
实验步骤 | 预期现象 |
步骤1:除铁。将铜粉置于烧杯中,__________________ | _______________________ |
步骤2:溶解。将步骤1得到的铜粉置于烧杯中, __________________________ | _______________________ |
步骤3:结晶。将步骤2所得溶液蒸发浓缩至液面有晶膜出现,冷却至室温,过滤得粗产品 |
|
(2)完成步骤1后,检验铜粉中的铁是否除尽的实验操作是___________。
(3)若胆矾中含有少量Cu(NO3)2·3H2O,测定其中CuSO4·5H2O的含量,实验步骤如下:称量胆矾样品的质量为m1,加水溶解,滴加足量BaCl2溶液,充分反应后过滤,将滤渣烘干、冷却,称得其质量为m2。样品中CuSO4·5H2O的质量分数为________(列出算式)。




