题目内容
在一个氧化还原反应体系中反应物、生成物共六种粒子,Fe3+、NO3-、Fe2+、NH4+、H+、H2O,下列叙述正确的是( )
| A、该反应说明Fe(NO3)2溶液不宜加酸酸化 | B、该反应中氧化剂与还原剂物质的量之比为8:1 | C、若有1mol NO3-发生氧化反应,转移电子5mol | D、若将该反应设计成原电池,则负极反应为Fe3++e-═Fe2+ |
分析:反应物、生成物共六种粒子,Fe3+、NO3-、Fe2+、NH4+、H+、H2O,发生NO3-+Fe2++H+→Fe3++NH4++H2O,Fe元素的化合价升高,N元素的化合价降低,以此来解答.
解答:解:A.硝酸盐在酸性条件下具有强氧化性,与亚铁离子反应,则该反应说明Fe(NO3)2溶液不宜加酸酸化,故A正确;
B.氧化剂为NO3-,还原剂为Fe2+,由电子守恒可知,氧化剂与还原剂物质的量之比为1:8,故B错误;
C.若有1mol NO3-发生氧化反应,转移电子为1mol×[5-(-3)]=8mol,故C错误;
D.若将该反应设计成原电池,则负极反应为Fe2+-e-═Fe3+,故D错误;
故选A.
B.氧化剂为NO3-,还原剂为Fe2+,由电子守恒可知,氧化剂与还原剂物质的量之比为1:8,故B错误;
C.若有1mol NO3-发生氧化反应,转移电子为1mol×[5-(-3)]=8mol,故C错误;
D.若将该反应设计成原电池,则负极反应为Fe2+-e-═Fe3+,故D错误;
故选A.
点评:本题考查氧化还原反应,为高频考点,把握离子的性质及习题信息中发生的氧化还原反应为解答的关键,注意从化合价角度分析,涉及基本概念及原电池设计等,题目难度中等.

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
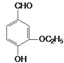 是食品添加剂的增香原料,其香味比香草醛更加浓郁.
是食品添加剂的增香原料,其香味比香草醛更加浓郁.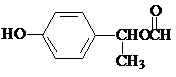 或
或
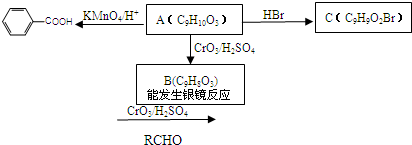
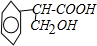

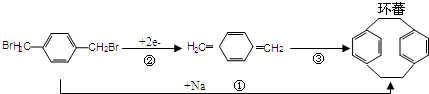
 ”结构的有机物不能稳定存在.请结合①②有关信息,分析如下转化关系,图中所用NaOH都是足量的,回答问题:
”结构的有机物不能稳定存在.请结合①②有关信息,分析如下转化关系,图中所用NaOH都是足量的,回答问题:



