题目内容
7.25℃时,0.001mol/L的NaOH溶液的pH等于( )| A. | 8 | B. | 9 | C. | 10 | D. | 11 |
分析 0.001mol/L的NaOH溶液中氢氧根离子浓度为0.001mol/L,根据c(H+)=$\frac{1{0}^{-14}}{c(O{H}^{-})}$计算出氢离子浓度,再计算出溶液的pH;
解答 解:NaOH为强电解质,则0.001mol/L的NaOH溶液中c(OH-)=0.001mol/L,c(H+)=$\frac{1{0}^{-14}}{c(O{H}^{-})}$mol/L=$\frac{1{0}^{-14}}{0.001}$mol/L=1×10-11mol/L,该氢氧化钠溶液的pH=-lg1×10-11=11,故选D.
点评 本题考查了溶液pH的计算,题目难度不大,注意掌握溶液酸碱性与溶液pH的计算方法,明确碱溶液的pH的计算方法,试题培养了学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
17.下列不能使有色布条褪色的物质是( )
| A. | 漂白粉溶液 | B. | 食盐水 | C. | 氯水 | D. | 次氯酸钠溶液 |
18.(1)已知短周期元素X的电离能数据如下(kJ•mol-1):
由X的电离能数据判断,X通常显+3价.
(2)单质硼有无定形和晶体两种,参考下表数据回答:
 ①晶体硼的晶体类型属于原子晶体,理由是熔、沸点很高、硬度很大,且各项数据介于金刚石和晶体硅之间.
①晶体硼的晶体类型属于原子晶体,理由是熔、沸点很高、硬度很大,且各项数据介于金刚石和晶体硅之间.
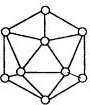
②已知晶体硼的结构单元是由硼原子组成的正二十面体(如图),其中有20个等边三角形的面和一定数目的顶角,每个顶角各有一个硼原子.通过观察图形及推算,得出此基本结构单元是由12个硼原子构成的,其中B-B键的键角为60°.
| 电离能 | I1 | I2 | I3 | I4 |
| X | 577 | 1817 | 2745 | 11578 |
(2)单质硼有无定形和晶体两种,参考下表数据回答:
| 金刚石 | 晶体硅 | 晶体硼 | |
| 熔点/K | <3823 | 1683 | 2573 |
| 沸点/K | 5100 | 2628 | 2823 |
| 硬度/Moh | 10 | 7.0 | 9.5 |
 ①晶体硼的晶体类型属于原子晶体,理由是熔、沸点很高、硬度很大,且各项数据介于金刚石和晶体硅之间.
①晶体硼的晶体类型属于原子晶体,理由是熔、沸点很高、硬度很大,且各项数据介于金刚石和晶体硅之间.②已知晶体硼的结构单元是由硼原子组成的正二十面体(如图),其中有20个等边三角形的面和一定数目的顶角,每个顶角各有一个硼原子.通过观察图形及推算,得出此基本结构单元是由12个硼原子构成的,其中B-B键的键角为60°.
15.有A、B、C三种金属,将A投入C的盐溶液中可置换出金属C,B的最高价氧化物的水化物碱性比A的最高价氧化物的水化物碱性强,则三种金属的金属性强弱顺序正确的是( )
| A. | A>B>C | B. | B>C>A | C. | B>A>C | D. | C>A>B |
2.能够用键能的大小作为主要依据来解释的是( )
| A. | CO2是直线形分子 | |
| B. | 稀有气体一般难发生化学反应 | |
| C. | 空气中氮气的化学性质比氧气稳定 | |
| D. | 常温常压下氯气呈气态而溴单质呈液态 |
12.下列叙述正确的是( )
| A. | 石油的催化裂化属于化学变化而裂解属于物理变化 | |
| B. | 煤的干馏属于物理变化 | |
| C. | 淀粉和纤维素在一定条件下水解均可得到葡萄糖 | |
| D. | 石油分馏得到的各馏分都是纯净物 |
19.在光照下,将等质量的CH4和Cl2充分反应,得到产物属于有机物的是( )
| A. | CH3Cl | B. | CH2Cl2 | C. | CHCl3 | D. | HCl |
16.下列说法中,正确的是( )
| A. | 燃着的酒精灯倒在桌上燃烧时赶紧把火吹灭 | |
| B. | 误食重金属盐立即喝大量生蛋清或鲜奶并及时洗胃 | |
| C. | 称量固体药品时,将药品直接放在天平托盘上 | |
| D. | 用高锰酸钾加热制取氧气结束时,先熄灭酒精灯,再从水槽中移出导气管 |
17.NH3是一种重要的化工原料,可以制备一系列物质(见图).下列说法正确的是( )


| A. | NH4Cl和NaHCO3都是常用的化肥 | |
| B. | NH4Cl、HNO3和Na2CO3受热时都易分解 | |
| C. | NH3和NO2在一定条件下可发生氧化还原反应 | |
| D. | 图中所涉及的盐类物质都属于正盐 |