题目内容
有原子序数依次增大的五种短周期元素A、B、C、D、E,已知 A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y;A、B、C、E四种元素,每种元素都能与D元素形成原子个数比不相同的常见化合物,回答下列问题:
(1)B在周期表中的位置是 ,C元素的单质的电子式
(2)写出同时含A、B、C、D四种元素的一种盐的化学式
(3)E和D形成的一种化合物与BD2发生氧化还原反应,该反应的方程式为
(4)在一定条件下,一定量的A的单质与C的单质反应,可生成17克气体化合物CA3,同时放出46kJ的热量,写出该反应的热化学方程式
(5)B、C两元素比较,非金属性较强的是 (填元素符号),用化学事实加以说明 (用化学方程式表示)
(1)B在周期表中的位置是
(2)写出同时含A、B、C、D四种元素的一种盐的化学式
(3)E和D形成的一种化合物与BD2发生氧化还原反应,该反应的方程式为
(4)在一定条件下,一定量的A的单质与C的单质反应,可生成17克气体化合物CA3,同时放出46kJ的热量,写出该反应的热化学方程式
(5)B、C两元素比较,非金属性较强的是
考点:位置结构性质的相互关系应用
专题:
分析:A、B、C、D、E为原子序数依次增大的五种短周期元素,A元素的原子半径最小,则A为H元素;
B元素原子的最外层电子数是内层电子数的2倍,最外层最多含有8个电子,则内层电子数为2,最外层电子数为4,故B为C盐酸;
C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,Y为硝酸铵,则C为N元素;
A、E同主族,根据原子序数大小可知E为Na元素;
A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物,则D为O元素,然后利用元素及其单质、化合物的性质来解答.
B元素原子的最外层电子数是内层电子数的2倍,最外层最多含有8个电子,则内层电子数为2,最外层电子数为4,故B为C盐酸;
C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,Y为硝酸铵,则C为N元素;
A、E同主族,根据原子序数大小可知E为Na元素;
A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物,则D为O元素,然后利用元素及其单质、化合物的性质来解答.
解答:
解:A、B、C、D、E为原子序数依次增大的五种短周期元素,A元素的原子半径最小,则A为H元素;B元素原子的最外层电子数是内层电子数的2倍,最外层最多含有8个电子,则内层电子数为2,最外层电子数为4,故B为C盐酸;C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,Y为硝酸铵,则C为N元素;A、E同主族,根据原子序数大小可知E为Na元素;A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物,则D为O元素,
(1)B为C元素,其原子序数为6,位于元素周期表中的第二周期第ⅣA族;C为N元素,对应单质为氮气,氮气分子中存在氮氮三键,氮气的电子式为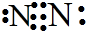 ,
,
故答案为:第二周期第ⅣA族;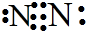 ;
;
(2)盐是由阳离子与酸根离子构成,A、B、C、D四种元素的两种盐的阳离子只能为铵根离子,则盐为NH4HCO3、CH3COONH4,
故答案为:NH4HCO3(或CH3COONH4);
(3)BD2为CO2,E和D形成的一种化合物能够与二氧化碳发生氧化还原反应,则该化合物为过氧化钠,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(4)氮气与氢气生成17g氨气放出46kJ的热量,则生成2molNH3放出92kJ的热量,则热化学反应方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92 kJ?mol-1,
故答案为:N2(g)+3H2(g)?2NH3(g)△H=-92 kJ?mol-1;
(5)B为C元素、C为N元素,二者位于同一周期,C的原子序数小于N,则非金属性N元素大于C元素;非金属性越强,最高价氧化物对应的水化物酸性越强,其非金属性越强,通过反应CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O可以证明N元素的非金属性大于C,
故答案为:N;CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O.
(1)B为C元素,其原子序数为6,位于元素周期表中的第二周期第ⅣA族;C为N元素,对应单质为氮气,氮气分子中存在氮氮三键,氮气的电子式为
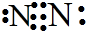 ,
,故答案为:第二周期第ⅣA族;
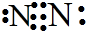 ;
;(2)盐是由阳离子与酸根离子构成,A、B、C、D四种元素的两种盐的阳离子只能为铵根离子,则盐为NH4HCO3、CH3COONH4,
故答案为:NH4HCO3(或CH3COONH4);
(3)BD2为CO2,E和D形成的一种化合物能够与二氧化碳发生氧化还原反应,则该化合物为过氧化钠,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(4)氮气与氢气生成17g氨气放出46kJ的热量,则生成2molNH3放出92kJ的热量,则热化学反应方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92 kJ?mol-1,
故答案为:N2(g)+3H2(g)?2NH3(g)△H=-92 kJ?mol-1;
(5)B为C元素、C为N元素,二者位于同一周期,C的原子序数小于N,则非金属性N元素大于C元素;非金属性越强,最高价氧化物对应的水化物酸性越强,其非金属性越强,通过反应CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O可以证明N元素的非金属性大于C,
故答案为:N;CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O.
点评:本题考查位置、结构、性质关系的综合应用,题目难度中等,正确推断各元素的名称为解答关键,注意掌握原子结构与元素周期表、元素周期律的关系.

练习册系列答案
相关题目
用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加快的是( )
| A、加热 |
| B、将稀硫酸改成98%的浓硫酸 |
| C、滴加少量CuSO4溶液 |
| D、不用铁片,改用铁粉 |
今有组成CH4O和C3H8O的混合物,在一定条件下进行脱水反应,可能生成的其它有机物的种数为( )
| A、5种 | B、6种 | C、7种 | D、8种 |
对化学反应限度的叙述,错误的是( )
| A、任何可逆反应都有一定的限度 |
| B、化学反应达到限度时,正逆反应速率相等 |
| C、化学反应的限度是不可改变的 |
| D、化学反应的限度与时间的长短无关 |
炒菜时,加一点酒和醋能使菜味香可口,原因是( )
| A、有酸类物质生成 |
| B、有醇类物质生成 |
| C、有酯类物质生成 |
| D、有盐类物质生成 |
下列组合中,中心离子的电荷数和配位数均相同的是( )
| A、K[Ag(CN)2]、[Cu(NH3)4]SO4 |
| B、[Ni(NH3)4]Cl2、[Cu(NH3)4]SO4 |
| C、[Ag(NH3)2]Cl、[Cu(NH3)2]Cl2 |
| D、[Ni(NH3)4]Cl2、[Ag(NH3)2]Cl |
能在水溶液中大量共存的一组离子是( )
| A、H+、I-、NO3-、SiO32- |
| B、Ag+、Na+、CO32-、SO42- |
| C、K+、SO42-、Cu2+、NO3- |
| D、NH4+、OH-、Cl-、HCO3- |
 (1、2-乙二醇)
(1、2-乙二醇)