题目内容
12.某化学小组拟采用如图所示装置(夹持和加热仪器已略去)来电解4mol/l食盐水,并用电解产生的H2还原CuO粉末,以此来测定Cu的相对原子质量.同时用产生的氢气与一氧化碳合成二甲醚.
请回答下列问题:
(1)配制本实验用到的4mol/LNaCl溶液250ml需NaCl固体质量58.5克,定容时俯视容量瓶将使所配溶液浓度大于4mol/L(“大于”、“等于”、“小于”)
(2)为完成上述实验,正确的连接顺序为A连E(填字母);电解发生的总的离子反应方程式为2H2O+2Cl-$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH-.
(3)通入氢气一段时间后,对硬质玻璃管里的CuO粉末加热前,需要进行的操作检验氢气的纯度.
(4)精确称量硬质玻璃管的质量为a g,放入CuO后,精确称量硬质玻璃管和CuO的总质量为b g,实验完毕后:通过精确称量U形管反应前后的质量,来确定生成水的质量d g,进而确定Cu的相对原子质量.利用U型管质量判断不再有水生成的方法是u型管质量至恒重(或连续两次称量质量之差小于0.1g)本实验有明显不足之处,请指出并提出改进意见空气中的CO2和水蒸气会通过D口进入U形管,从而产生较大的实验误差.若不改进将使测定结果偏低(“偏高”、“偏低”、“无影响”).根据以上数据计算铜的相对原子质量$\frac{18(b-a)}{d}-16$.
分析 (1)根据质量m=CVM来计算;定容时俯视液面会使溶液体积偏小;
(2)由于A所在的极为阴极,电极反应为:2H2O+2e-=H2↑+2OH-,然后根据实验目的是用电解产生的H2还原CuO粉末,据此分析A所连的导管;电解饱和食盐水时,阳极上Cl-放电,阴极上H+放电,据此分析;
(3)此实验是用氢气来还原CuO,若加热的是氢气和空气的混合物,在易发生爆炸;
(4)实验原理是将氢气通过E进入C中的浓硫酸进行干燥,故通到硬质玻璃管中后,在加热条件下能将CuO还原为Cu,并生成水蒸汽,从而被b中的碱石灰吸收,即硬质玻璃管的减重量即为CuO中的含有的氧原子的质量,b的增重量即为H2O的质量,据此分析.
解答 解:(1)所需的氯化钠的质量m=CVM=4mol/L×0.25L×58.5g/mol=58.5g;定容时俯视液面会使溶液体积偏小,则浓度偏大,故答案为:58.5,大于;
(2)由于A所在的极为阴极,电极反应为:2H2O+2e-=H2↑+2OH-,故从A导出的气体是氢气,由于本实验的目的是用电解产生的H2还原CuO粉末,故要将从A中出来的气体先经浓硫酸干燥,然后通入CuO固体上,故A所连的导管应为E;电解饱和食盐水时,阳极上Cl-放电:2Cl-+2e-=Cl2,阴极上H+放电:2H2O+2e-=H2↑+2OH-,故电解的总反应为:2H2O+2Cl-$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH-,故答案为:E,2H2O+2Cl-$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH-;
(3)此实验是用氢气来还原CuO,若加热的是氢气和空气的混合物,在易发生爆炸,故在加热前应先检验氢气的纯度,故答案为:检验氢气的纯度;
(4)实验原理是将氢气通过E进入C中的浓硫酸进行干燥,故通到硬质玻璃管中后,在加热条件下能将CuO还原为Cu,并生成水蒸汽,从而被b中的碱石灰吸收,即硬质玻璃管的减重量即为CuO中的含有的氧原子的质量,b的增重量即应为生成H2O的质量.
故当U型管质量的质量不再变化时,说明CuO中的氧元素已经完全被结合生成水,即不再有水生成;但由于空气中的水蒸气和二氧化碳能通过D进入b从而被吸收,故b增重的质量偏大,导致产生误差;若不改变,则会导致生成水的质量偏高,则测得的CuO中氧原子的质量偏多,故Cu原子的质量偏小,则铜的相对原子质量偏低;
由于生成水的质量为dg,故水的物质的量为n=$\frac{d}{18}$mol,故CuO中氧原子的质量为m=$\frac{d}{18}mol×16g/mol$=$\frac{16d}{18}$g,由于CuO的质量为(b-a)g,故CuO中含有的铜原子的质量为:
(b-a)g-$\frac{16d}{18}$g=$\frac{18(b-a)-16d}{18}$g.由于水的物质的量为$\frac{d}{18}mol$,而其中的氧原子来自于CuO,物质的量也为$\frac{d}{18}mol$,而在CuO中,铜原子和氧原子的物质的量之比为1:1,故含有的铜原子的物质的量也为$\frac{d}{18}mol$,则铜原子的摩尔质量为M=$\frac{m}{n}$=$\frac{\frac{18(b-a)-16d}{18}g}{\frac{d}{18}mol}$=$\frac{18(b-a)}{d}-16$g/mol,即铜的相对原子质量为$\frac{18(b-a)}{d}-16$.
故答案为:u型管质量至恒重(或连续两次称量质量之差小于0.1g);空气中的CO2和水蒸气会通过D口进入U形管;从而产生较大的实验误差; 偏低;$\frac{18(b-a)}{d}-16$.
点评 本题考查了物质性质的验证和物质测定实验设计方案,物质性质的掌握,实验步骤和实验原理的理解是解题关键,题目难度中等.

 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案| A. |  分液漏斗 | B. |  酒精灯 | C. |  锥形瓶 | D. |  容量瓶 |
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
| 其它 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
(2)Z的单质与水反应的离子方程式是2Na+2H2O=2Na++2OH-+H2↑.
(3)Y与R相比,非金属性较强的是Cl(用元素符号表示),下列事实能证明这一结论的是bc(选填字母序号).
a.常温下Y的单质呈固态,R的单质呈气态 b.稳定性XR>YX4
c.Y与R形成的化合物中Y呈正价 d.沸点XR>YX4
(4)根据表中数据推测,Y的原子半径的最小范围是0.099nm<r(Si)<0.143nm.
(5)X、M、R形成的能够杀菌、消毒物质的结构式为H-O-Cl.
(6)甲、乙是上述部分元素的最高价氧化物的水化物,且甲+乙→丙+水.若丙的水溶液呈碱性,则丙的化学式是NaAlO2.
| A. | 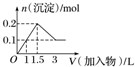 向1L浓度均为0.1 mol•L-1的Ba(OH)2、NaAlO2混合溶液中加入0.1 mol•L-1的稀H2SO4 | |
| B. | 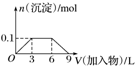 向1L浓度分别为0.1 mol•L-1和0.3 mol•L-1的AlCl3、NH4Cl的混合溶液中加入0.1 mol•L-1的稀NaOH溶液 | |
| C. | 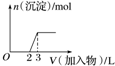 向烧碱溶液中滴加明矾溶液 | |
| D. | 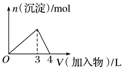 向AlCl3溶液中滴加过量氨水 |
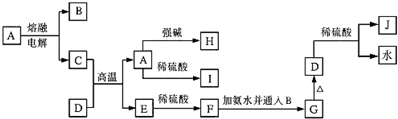
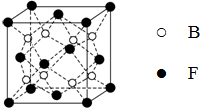 已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素,A与B;C、D与E分别位于同一周期.A原子L层上有2对成对电子,B、C、D的核外电子排布相同的简单离子可形成一种C3DB6型离子晶体X,CE、FA为电子数相同的离子晶体.
已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素,A与B;C、D与E分别位于同一周期.A原子L层上有2对成对电子,B、C、D的核外电子排布相同的简单离子可形成一种C3DB6型离子晶体X,CE、FA为电子数相同的离子晶体.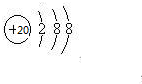 ,X的化学式Na3AlF6.
,X的化学式Na3AlF6.