题目内容
下列离子方程式中正确的是( )
| A、氯化铝溶液中加入过量氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、AlCl3 溶液中投入过量Na:Al3++4Na+2H2O=AlO2-+4Na++2H2↑ |
| C、苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
| D、碳酸氢铵溶液中加入过量氢氧化钠溶液:HCO3-+OH-=CO32-+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.氢氧化铝能溶于强碱但不溶于弱碱;
B.钠和水反应生成NaOH和氢气,过量NaOH再和氯化铝反应生成偏铝酸钠和水;
C.苯酚的酸性小于碳酸,所以苯酚钠和二氧化碳、水反应生成苯酚和碳酸氢钠;
D.碳酸氢铵和过量NaOH溶液反应生成一水合氨、碳酸钠和水.
B.钠和水反应生成NaOH和氢气,过量NaOH再和氯化铝反应生成偏铝酸钠和水;
C.苯酚的酸性小于碳酸,所以苯酚钠和二氧化碳、水反应生成苯酚和碳酸氢钠;
D.碳酸氢铵和过量NaOH溶液反应生成一水合氨、碳酸钠和水.
解答:
解:A.氢氧化铝能溶于强碱但不溶于弱碱,离子方程式为Al3++3NH3?H2O=Al(OH)3↓+3 NH4+,故A错误;
B.钠和水反应生成NaOH和氢气,过量NaOH再和氯化铝反应生成偏铝酸钠和水,离子方程式为Al3++4Na+2H2O=AlO2-+4Na++2H2↑,故B正确;
C.苯酚的酸性小于碳酸,所以苯酚钠和二氧化碳、水反应生成苯酚和碳酸氢钠,离子方程式为C6H5O-+CO2+H2O→C6H5OH+HCO3-,故C错误;
D.碳酸氢铵和过量NaOH溶液反应生成一水合氨、碳酸钠和水,离子方程式为NH4++HCO3-+2OH-═CO32-+H2O+NH3.H2O,故D错误;
故选B.
B.钠和水反应生成NaOH和氢气,过量NaOH再和氯化铝反应生成偏铝酸钠和水,离子方程式为Al3++4Na+2H2O=AlO2-+4Na++2H2↑,故B正确;
C.苯酚的酸性小于碳酸,所以苯酚钠和二氧化碳、水反应生成苯酚和碳酸氢钠,离子方程式为C6H5O-+CO2+H2O→C6H5OH+HCO3-,故C错误;
D.碳酸氢铵和过量NaOH溶液反应生成一水合氨、碳酸钠和水,离子方程式为NH4++HCO3-+2OH-═CO32-+H2O+NH3.H2O,故D错误;
故选B.
点评:本题考查离子方程式正误判断,明确离子性质及离子方程式书写规则即可解答,注意有些反应与反应物的量、浓度有关,易错选项是C,注意无论二氧化碳量多少都生成碳酸氢钠,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
甲烷分子是以碳原子为中心的正四面体形结构,而不是正方形的平面结构,理由是( )
| A、CH3Cl只有一种空间结构 |
| B、CH2Cl2只有一种空间结构 |
| C、CHCl3只有一种空间结构 |
| D、CCl4是非极性分子 |
氧化性随原子序数的增加而增强的是( )
| A、F-、Cl-、Br- |
| B、Na+、Mg2+、Al3+ |
| C、P、S、Cl |
| D、Li+、Na+、K+ |
下列离子方程式中正确的是( )
| A、用氯化铁溶液腐蚀铜板:Fe3++Cu=Fe2++Cu2+ |
| B、将少量的二氧化硫气体通入次氯酸钠溶液中 SO2+H2O+2ClO-=SO32-+2HClO |
| C、用氢氧化钡溶液中和硫酸氢铵溶液:H++SO42-+Ba2++OH-=H2O+BaSO4↓ |
| D、用纯碱溶液溶解苯酚:CO32-+C6H5OH→HCO3-+C6H5O- |
能正确表示下列反应的离子方程式是( )
| A、铁跟硫酸铜溶液反应:2Fe+3Cu2+=2Fe3++3Cu |
| B、饱和石灰水跟稀硝酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| C、在碳酸氢钙溶液中加入盐酸:CO32-+2H+=CO2↑+H2O |
| D、在澄清石灰水里通入过量二氧化碳:OH-+CO2=HCO3- |
一定能够鉴定卤代烃中卤元素的存在的操作是( )
| A、在卤代烃中直接加入AgNO3溶液 |
| B、加蒸馏水,充分搅拌后,加入AgNO3溶液 |
| C、加入NaOH溶液,加热后加入稀硝酸酸化,再加入AgNO3溶液 |
| D、加入NaOH的乙醇溶液,加热后加入AgNO3溶液 |
能用酒精灯直接加热的一组仪器是( )
| A、坩埚、蒸发皿 |
| B、烧瓶、蒸发皿 |
| C、试管、锥形瓶 |
| D、试管、烧杯 |
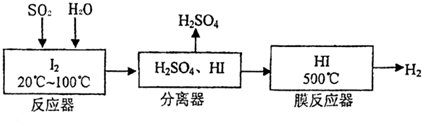

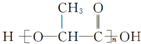 ,有关W的信息如图,据此回答下列问题:
,有关W的信息如图,据此回答下列问题: