题目内容
25℃时某溶液中,由水电离出的c(H+)和c(OH-)的乘积为1×10-26,下列有关说法中正确的是( )
| A、该溶液中的溶质不可能是NaHSO4 | ||
| B、向该溶液中加入铝粉,一定能产生大量H2 | ||
C、下列离子在该溶液中一定能大量共存:Ca2+、Cl-、K+、NO
| ||
| D、向该溶液中加入NaHCO3,一定有化学反应发生 |
考点:水的电离
专题:电离平衡与溶液的pH专题
分析:25℃时某溶液中,水电离出的c(H+)和c(OH-)的乘积是1×10-26,由于c(H+)和c(OH-)的乘积小于10-14,说明水的电离受到了抑制,其溶质只能是酸或碱,据此进行判断.
解答:
解:依据分析可知,溶液可能是酸或碱溶液对水的电离起到抑制作用,
A、NaHSO4 溶液中完全电离,生成氢离子溶液显酸性,对水的电离起到抑制作用,故A错误;
B、溶液是酸或碱,向该溶液中加入铝粉,若是硝酸,不能产生大量H2,故B错误;
C、氢氧化钙是微溶于水的物质,碱溶液中Ca2+和氢氧根离子浓度达到溶度积常数会生成氢氧化钙沉淀,故C错误;
D、NaHCO3是弱酸的酸式盐和碱反应生成盐和水,HCO3-+OH-=CO32-+H2O,和酸反应生成二氧化碳和水,HCO3-+H+=CO2↑+H2O,故D正确;
故选D.
A、NaHSO4 溶液中完全电离,生成氢离子溶液显酸性,对水的电离起到抑制作用,故A错误;
B、溶液是酸或碱,向该溶液中加入铝粉,若是硝酸,不能产生大量H2,故B错误;
C、氢氧化钙是微溶于水的物质,碱溶液中Ca2+和氢氧根离子浓度达到溶度积常数会生成氢氧化钙沉淀,故C错误;
D、NaHCO3是弱酸的酸式盐和碱反应生成盐和水,HCO3-+OH-=CO32-+H2O,和酸反应生成二氧化碳和水,HCO3-+H+=CO2↑+H2O,故D正确;
故选D.
点评:本题考查了水的电离、水的离子积常数,题目难度中等,注意水电离的氢离子与溶液酸碱性的关系.

练习册系列答案
相关题目
下列有关化学用语使用正确的是( )
A、CH4分子的比例模型: |
| B、乙醇的分子式CH3CH2OH |
| C、苯的最简式 C6H6 |
| D、乙烯的结构简式CH2CH2 |
下列叙述与盐类水解无关的是( )
| A、草木灰与磷肥混合使用会降低肥效 |
| B、使用明矾、氯化铁作净水剂 |
| C、碳酸钙加入水中导电性很弱 |
| D、用硫酸铝和小苏打溶液制泡沫灭火器 |
下列有机反应的化学方程式和反应类型均正确的是( )
A、CH4+Cl2
| ||
B、nCH3-CH=CH2
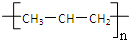 聚合反应 聚合反应 | ||
C、淀粉:(C6H10O5)n+nH2O
| ||
D、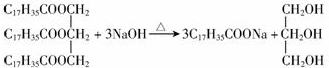 皂化反应 皂化反应 |
下列说法中错误的是( )
| A、能量变化是化学反应的基本特征之一 |
| B、化学反应都伴随着能量变化和其他各种现象的出现 |
| C、拆开物质中的化学键一定需要吸收能量 |
| D、形成化学键的过程一定释放能量 |
下列命名或说法正确的是( )
A、 的名称是2,5,6-三甲基-4-乙基庚烷 的名称是2,5,6-三甲基-4-乙基庚烷 |
| B、常压下,正戊烷、异戊烷、新戊烷的沸点依次增大 |
C、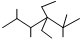 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 |
| D、2,3-二甲基-1-丁烯 |
下列物质所属的类别正确的是( )
| A、Na2CO3--盐 |
| B、干冰--混合物 |
| C、氢氧化铁胶体--纯净物 |
| D、NaHCO3--酸 |
浓硫酸具有的性质是( )
| A、强的氧化性 | B、碱性 |
| C、还原性 | D、两性 |