题目内容
甲和乙反应生成丙的过程如下图所示,下列叙述正确的是( )


| A、参加反应的甲和生成的丙的物质的量之比1:1 |
| B、丙中碳和氢两种元素的质量比为1:3 |
| C、该反应属于复分解反应 |
| D、甲、乙、丙都是有机物 |
考点:球棍模型与比例模型
专题:有机物分子组成通式的应用规律
分析:由示意图可知甲、乙、丙分别为H2O、CH2=CH2、CH3CH2OH,如图所示的反应为H2O+CH2=CH2→CH3CH2OH.
解答:
解:由示意图可知甲、乙、丙分别为H2O、CH2=CH2、CH3CH2OH,如图所示的反应为H2O+CH2=CH2→CH3CH2OH.
A、有反应H2O+CH2=CH2→CH3CH2OH知甲和丙的物质的量之比为1:1,故A正确;
B、丙中碳和氢两种元素的质量比为12g/mol×2:1g/mol×6=4:1,故B错误;
C、H2O+CH2=CH2→CH3CH2OH属于加成反应,故C错误;
D、甲为H2O,属于无机物,故D错误.
故选:A.
A、有反应H2O+CH2=CH2→CH3CH2OH知甲和丙的物质的量之比为1:1,故A正确;
B、丙中碳和氢两种元素的质量比为12g/mol×2:1g/mol×6=4:1,故B错误;
C、H2O+CH2=CH2→CH3CH2OH属于加成反应,故C错误;
D、甲为H2O,属于无机物,故D错误.
故选:A.
点评:通过球棍模型或比例模型判断选项的正误要看准图形符号表示的化学意义,本题难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列有机反应中,不属于取代反应的是( )
A、CH3COOH+CH3CH2OH
| |||
B、2CH3CH2OH
| |||
C、CH3CH2OH
| |||
D、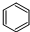 +Br2 +Br2
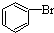 +HBr +HBr |
根据如图海水综合利用的工业流程图,判断下列说法正确的是( )已知:MgCl2?6H2O受热生成Mg(OH)Cl和HCl气体等
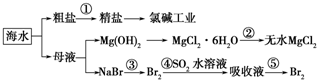

| A、除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 |
| B、在过程②中将MgCl2?6H2O灼烧即可制得无水MgCl2 |
| C、从能量转换角度来看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程 |
| D、从第③步到第⑤步的目的是为了浓缩 |
100g物质的量浓度为18.4mol/L,质量分数为98%的浓硫酸,与100mL水混合后,得到质量分数为49%的稀硫酸,该稀硫酸的物质的量浓度为c2的值可能为( )
| A、=9.2mol/L |
| B、>9.2mol/L |
| C、<9.2mol/L |
| D、=9.8mol/L |
下列实验装置设计正确的是( )
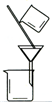
A、 干燥氯气 |
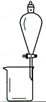
B、 稀释浓硫酸 |
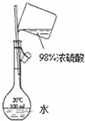
C、 实验室制氨气 |
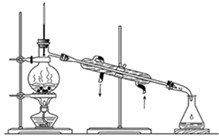
D、 分馏石油 |
下列物质中,属于电解质的是( )
| A、硫酸钠 | B、铜 |
| C、二氧化碳 | D、盐酸 |
20℃时,饱和KCl溶液的密度为1.174g?cm-3,物质的量浓度为4.0mol?L-1,则下列说法中不正确的是( )
| A、25℃时,饱和KCl溶液的浓度大于4.0 mol?L-1 |
| B、20℃时,饱和KCl溶液的质量分数为25.4% |
| C、20℃时,密度小于1.174g?cm-3的KCl溶液是不饱和溶液 |
| D、20℃时,KCl的溶解度为34.0% |
已知:Li与Mg、Be与Al的性质相似.下列判断正确的是( )
| A、LiOH是强碱 |
| B、Be与冷水剧烈反应 |
| C、Li在空气中不易被氧化 |
| D、Be(OH)2能与NaOH溶液反应 |