题目内容
 将镁铝的混合物0.1mol溶于100mL 2mol?L-1硫酸溶液中,然后再滴加1mol?L-1氢氧化钠溶液,请回答以下问题:
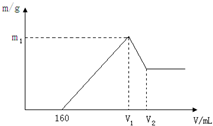
将镁铝的混合物0.1mol溶于100mL 2mol?L-1硫酸溶液中,然后再滴加1mol?L-1氢氧化钠溶液,请回答以下问题:(1)若在滴加NaOH溶液的过程中,产生沉淀的质量m随加入NaOH溶液的体积变化如图所示,则V1=
(2)若混合物仍为0.1mol,其中镁的物质的量分数为a,用100mL2mol?L-1硫酸溶解后,再加入450mL 1mol?L-1氢氧化钠溶液,所得溶液无Al(OH)3沉淀.满足此条件的a的取值范围是
考点:镁、铝的重要化合物,化学方程式的有关计算
专题:图示题
分析:(1)镁铝的混合物溶于稀硫酸溶液中,发生反应生成硫酸镁和硫酸铝,然后再滴入氢氧化钠溶液,氢氧化钠体积小于160ml时,和没有反应的硫酸反应,故0~160ml时,不产生沉淀,氢氧化钠体积为160ml~v1时,硫酸镁和硫酸铝和氢氧化钠反应生成氢氧化镁和氢氧化铝,氢氧化钠体积为v1~v2时氢氧化铝和氢氧化钠反应,生成偏铝酸钠,当氢氧化钠体积为v1时,镁离子和铝离子恰好沉淀,溶液中阳离子为Na+,阴离子为SO42-,即溶液中的溶质为Na2SO4,n(Na+)=2n(SO42-),其中Na+来自NaOH,SO42-来自H2SO4,故当氢氧化钠体积为v1时,n(NaOH)=2n(H2SO4);
(2)若混合物仍为0.1mol,其中镁的物质的量分数为a,用100mL2mol?L-1硫酸溶解后,再加入450mL 1mol?L-1氢氧化钠溶液,所得溶液无Al(OH)3沉淀,证明生成的氢氧化铝全部和氢氧化钠反应,由上述分析知:v1=400ml,再加入50mL 1mol?L-1氢氧化钠溶液,所得Al(OH)3沉淀完全溶于氢氧化钠生成偏铝酸钠,所得Al(OH)3沉淀完全溶于氢氧化钠生成偏铝酸钠,求得:Al(OH)3最大取值0.05mol,即0<n(Al)≤0.05mol,n(Mg)+n(Al)=0.1mol,则0.5≤n(Mg)<1.
(2)若混合物仍为0.1mol,其中镁的物质的量分数为a,用100mL2mol?L-1硫酸溶解后,再加入450mL 1mol?L-1氢氧化钠溶液,所得溶液无Al(OH)3沉淀,证明生成的氢氧化铝全部和氢氧化钠反应,由上述分析知:v1=400ml,再加入50mL 1mol?L-1氢氧化钠溶液,所得Al(OH)3沉淀完全溶于氢氧化钠生成偏铝酸钠,所得Al(OH)3沉淀完全溶于氢氧化钠生成偏铝酸钠,求得:Al(OH)3最大取值0.05mol,即0<n(Al)≤0.05mol,n(Mg)+n(Al)=0.1mol,则0.5≤n(Mg)<1.
解答:
解:镁铝的混合物溶于稀硫酸溶液中,发生反应生成硫酸镁和硫酸铝,然后再滴入氢氧化钠溶液,氢氧化钠体积小于160ml时,和没有反应的硫酸反应,故0~160ml时,不产生沉淀,氢氧化钠体积为160ml~v1时,硫酸镁和硫酸铝和氢氧化钠反应生成氢氧化镁和氢氧化铝,氢氧化钠体积为v1~v2时氢氧化铝和氢氧化钠反应,生成偏铝酸钠;
当氢氧化钠体积为v1时,镁离子和铝离子恰好沉淀,溶液中阳离子为Na+,阴离子为SO42-,即溶液中的溶质为Na2SO4,n(Na+)=2n(SO42-),其中Na+来自NaOH,SO42-来自H2SO4,故当氢氧化钠体积为v1时,n(NaOH)=2n(H2SO4)=2×2mol?L-1×0.1L=0.4mol,v(NaOH)=
=
=0.4L=400ml;故v1=400ml;
(1)设0.1mol镁铝的混合物中镁、铝的物质的量分别为x和y,x+y=0.1mol①,
氢氧化钠体积小于160ml时不产生沉淀,此时氢氧化钠和没有反应的硫酸反应,和硫酸反应的氢氧化钠物质的量=0.16L×1mol?L-1=0.16mol,
2NaOH+H2SO4=Na2SO4+2H2O
0.16mol 0.08mol
镁铝和硫酸反应,消耗的硫酸应该为:0.1L×2mol?L-1-0.08mol=0.12mol
发生的反应分别为:Mg+H2SO4=MgSO4+H2,2Al+3H2SO4=Al2(SO4)3+3H2,
x x y
y
则:x+
y═0.12mol②
由式①②可得x=0.06mol,y=0.04mol;即镁、铝的物质的量分别为0.06mol和0.04mol,氢氧化钠体积为v1时生成Mg(OH)2和Al(OH)3物质的量分别0.06mol和0.04mol;
氢氧化钠体积为v1~v2时氢氧化铝和氢氧化钠反应,生成偏铝酸钠,Al(OH)3 +NaOH=NaAlO2+2H2O,
0.04mol 0.04mol
Al(OH)3 和NaOH反应消耗NaOH0.04mol,v(NaOH)=
=
=0.04L=40ml;即:v1~v2时氢氧化钠为40ml,0~v1消耗400ml氢氧化钠,V2=440 mL;
Mg~~Mg(OH)2 ; Al~~Al(OH)3;
0.06mol 0.06mol 0.04mol 0.04mol
在滴加NaOH溶液的过程中,产生沉淀的质量m=m(Mg(OH)2 )+m(Al(OH)3)=0.06mol×58g/mol+0.04mol×78g/mol=6.6g
故答案为:V1=400 mL;V2=440 mL;m1=6.6 g;
(2)若混合物仍为0.1mol,其中镁的物质的量分数为a,用100mL2mol?L-1硫酸溶解后,再加入450mL 1mol?L-1氢氧化钠溶液,所得溶液无Al(OH)3沉淀,证明生成的氢氧化铝全部和氢氧化钠反应,由上述分析知:v1=400ml,再加入50mL 1mol?L-1氢氧化钠溶液,所得Al(OH)3沉淀完全溶于氢氧化钠生成偏铝酸钠,Al(OH)3 +NaOH=NaAlO2+2H2O,Al(OH)3最大取值0.05mol,即0<n(Al)≤0.05mol,n(Mg)+n(Al)=0.1mol,则0.5≤n(Mg)<1
0.05 0.05
故答案为:0.5≤a<1.
当氢氧化钠体积为v1时,镁离子和铝离子恰好沉淀,溶液中阳离子为Na+,阴离子为SO42-,即溶液中的溶质为Na2SO4,n(Na+)=2n(SO42-),其中Na+来自NaOH,SO42-来自H2SO4,故当氢氧化钠体积为v1时,n(NaOH)=2n(H2SO4)=2×2mol?L-1×0.1L=0.4mol,v(NaOH)=
| n(NaOH) |
| c(NaOH) |
| 0.4mol |
| 1mol?L-1 |
(1)设0.1mol镁铝的混合物中镁、铝的物质的量分别为x和y,x+y=0.1mol①,
氢氧化钠体积小于160ml时不产生沉淀,此时氢氧化钠和没有反应的硫酸反应,和硫酸反应的氢氧化钠物质的量=0.16L×1mol?L-1=0.16mol,
2NaOH+H2SO4=Na2SO4+2H2O
0.16mol 0.08mol
镁铝和硫酸反应,消耗的硫酸应该为:0.1L×2mol?L-1-0.08mol=0.12mol
发生的反应分别为:Mg+H2SO4=MgSO4+H2,2Al+3H2SO4=Al2(SO4)3+3H2,
x x y
| 3 |
| 2 |
则:x+
| 3 |
| 2 |
由式①②可得x=0.06mol,y=0.04mol;即镁、铝的物质的量分别为0.06mol和0.04mol,氢氧化钠体积为v1时生成Mg(OH)2和Al(OH)3物质的量分别0.06mol和0.04mol;
氢氧化钠体积为v1~v2时氢氧化铝和氢氧化钠反应,生成偏铝酸钠,Al(OH)3 +NaOH=NaAlO2+2H2O,
0.04mol 0.04mol
Al(OH)3 和NaOH反应消耗NaOH0.04mol,v(NaOH)=
| n(NaOH) |
| c(NaOH) |
| 0.04mol |
| 1mol?L-1 |
Mg~~Mg(OH)2 ; Al~~Al(OH)3;
0.06mol 0.06mol 0.04mol 0.04mol
在滴加NaOH溶液的过程中,产生沉淀的质量m=m(Mg(OH)2 )+m(Al(OH)3)=0.06mol×58g/mol+0.04mol×78g/mol=6.6g
故答案为:V1=400 mL;V2=440 mL;m1=6.6 g;
(2)若混合物仍为0.1mol,其中镁的物质的量分数为a,用100mL2mol?L-1硫酸溶解后,再加入450mL 1mol?L-1氢氧化钠溶液,所得溶液无Al(OH)3沉淀,证明生成的氢氧化铝全部和氢氧化钠反应,由上述分析知:v1=400ml,再加入50mL 1mol?L-1氢氧化钠溶液,所得Al(OH)3沉淀完全溶于氢氧化钠生成偏铝酸钠,Al(OH)3 +NaOH=NaAlO2+2H2O,Al(OH)3最大取值0.05mol,即0<n(Al)≤0.05mol,n(Mg)+n(Al)=0.1mol,则0.5≤n(Mg)<1
0.05 0.05
故答案为:0.5≤a<1.
点评:本题考查镁铝化合物性质、混合物的计算,以图象题的形式考查,题目难度中等,分析图象各阶段的发生的反应是解题关键,

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
用导线将铜片和锌片连接后插入稀硫酸中组成原电池,其中锌片作( )
| A、阳极 | B、阴极 | C、正极 | D、负极 |
下列叙述不正确的是( )
| A、Na、Mg、Al元素最高化合价依次升高 |
| B、P、S、Cl元素最高价氧化物对应的水化物酸性依次增强 |
| C、N、O、F元素非金属性依次减弱 |
| D、Li、Na、K原子的电子层数依次增多 |
下列解释事实的方程式不准确的是( )
| A、绿矾久存,表面变黄褐色:4(FeSO4?7H2O)+O2=4Fe(OH)SO4+26H2O |
| B、不能用玻璃塞试剂瓶盛放强碱性溶液:SiO2+2OH-=SiO32-+H2O |
| C、淡黄色的过氧化钠粉末久存,表面变白:2Na2O2=2Na2O+O2 |
| D、长期盛放石灰水的试剂瓶内壁出现白色固体:Ca(OH)2+CO2=CaCO3↓+H2O |