题目内容
1.常温下,下列指定溶液中一定能大量共存的是( )| A. | 无色透明溶液中:K+、Cu2+、SO42-、Na+ | |
| B. | pH=12的溶液中:K+、Na+、SO42-、CH3COO-、CO32- | |
| C. | 加入铝片能放出H2的溶液中:Na+、HCO3-、Cu2+、SO42- | |
| D. | 由水电离出的c(H+)=1×10-12 mol/L的溶液中:NH4+、Ba2+、NO3-、Cl- |
分析 A.铜离子为有色离子;
B.pH=12的溶液中存在电离氢氧根离子,5种离子之间不反应,都不与氢氧根离子反应;
C.加入铝片能放出H2的溶液中存在大量氢离子或氢氧根离子,碳酸氢根离子、铜离子之间发生双水解反应,铁离子与氢氧根离子反应,碳酸氢根离子与氢离子和氢氧根离子反应;
D.由水电离出的c(H+)=1×10-12 mol/L的溶液为酸性或碱性溶液,铵根离子与氢氧根离子反应.
解答 解:A.Cu2+为有色离子,在溶液中不能大量共存,故A错误;
B.pH=12的溶液为碱性溶液,溶液中存在大量氢氧根离子,K+、Na+、SO42-、CH3COO-、CO32-之间不反应,都不与氢氧根离子反应,在溶液中能够大量共存,故B正确;
C.加入铝片能放出H2的溶液为酸性或强碱性溶液,溶液中存在大量氢离子或氢氧根离子,HCO3-、Cu2+之间发生双水解反应,HCO3-、Cu2+都与氢氧根离子反应,HCO3-与氢离子反应,在溶液中一定不能大量共存,故C错误;
D.由水电离出的c(H+)=1×10-12 mol/L的溶液中存在大量氢离子或氢氧根离子,NH4+与氢氧根离子反应,在碱性溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,题目难度中等,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等;试题侧重对学生基础知识的训练和检验,有利于提高学生灵活运用基础知识的能力.

练习册系列答案
相关题目
11.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 1mol H2O含有的原子数为NA | |
| B. | 4gH2含有氢分子数4NA | |
| C. | 常温常压下,11.2L O2中含有分子数为0.5NA | |
| D. | 1L 0.1 mol•L-1NaCl溶液中含Na+数0.1NA |
12.下列溶液中氯离子浓度最小的是( )
| A. | 150ml 1mol/L的NaCl溶液 | B. | 150ml 3mol/LKCl溶液 | ||
| C. | 75ml 2mol/L的NH4Cl溶液 | D. | 50ml 1mol/lCuCl2溶液 |
9.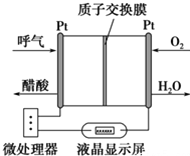 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )
如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )
 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )
如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )| A. | 该电池的负极反应式为:CH3CH2OH+3H2O-12e-═2CO2↑+12H+ | |
| B. | 该电池的正极反应式为:O2+4e-+4H+═2H2O | |
| C. | 电流由O2所在的铂电极经外电路流向另一电极 | |
| D. | 微处理器通过检测电流大小而计算出被测气体中酒精的含量 |
16.关于化学反应 Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO 叙述正确的是( )
| A. | 上述反应中,N2是还原剂,Al2O3是氧化剂 | |
| B. | 上述反应中,每生成1 mol AlN需转移3 mol电子 | |
| C. | AlN中氮元素的化合价为+3价 | |
| D. | AlN的摩尔质量为41 g |
6.短周期元素的四种离子A2+、B+、C2-、D-具有相同电子层结构,下列叙述正确的是( )
| A. | 原子序数:D>C>B>A | B. | 氢化物的稳定性:H2C>HD | ||
| C. | 离子半径:C2->D->B+>A2+ | D. | 氧化性:A2+>B+,还原性:C2-<D- |
13.已知热化学方程式:
①C2H2(g)+O2(g)═2CO2(g)+H2O(l)△H1=-1301.0kJ•mol-1
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ•mol-1
③H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H3=-285.8kJ•mol-1
则反应④2C(s)+H2(g)═C2H2(g)的△H为( )
①C2H2(g)+O2(g)═2CO2(g)+H2O(l)△H1=-1301.0kJ•mol-1
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ•mol-1
③H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H3=-285.8kJ•mol-1
则反应④2C(s)+H2(g)═C2H2(g)的△H为( )
| A. | +228.2 kJ•mol-1 | B. | -228.2 kJ•mol-1 | ||
| C. | +1 301.0 kJ•mol-1 | D. | +621.7 kJ•mol-1 |
10.将海水淡化和与浓海水资源化结合起来是综合利用海水的重要途径之一.一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺提取其他产品.回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是②③④(填序号).
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾.溴.镁的提取工艺
(2)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸收.碱吸收溴的主要反应是:Br2+Na2CO3+H2O→NaBr+NaBrO3+6NaHCO3,吸收1mol Br2时转移的电子为$\frac{5}{3}$mol.
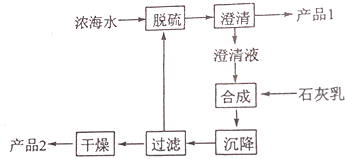
(3)海水提镁的一段工艺流程如图:浓海水的主要成分如下:
该工艺过程中,脱硫阶段主要反应的离子方程式为Ca2++SO42-=CaSO4↓,产品2的化学式为Mg(OH)2,1L浓海水最多可得到产品2的质量为69.6g.
(4)采用石墨阳极.不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式Mg+2H2O$\frac{\underline{\;高温\;}}{\;}$Mg(OH)2+H2↑.

(1)下列改进和优化海水综合利用工艺的设想和做法可行的是②③④(填序号).
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾.溴.镁的提取工艺
(2)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸收.碱吸收溴的主要反应是:Br2+Na2CO3+H2O→NaBr+NaBrO3+6NaHCO3,吸收1mol Br2时转移的电子为$\frac{5}{3}$mol.
(3)海水提镁的一段工艺流程如图:浓海水的主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
(4)采用石墨阳极.不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式Mg+2H2O$\frac{\underline{\;高温\;}}{\;}$Mg(OH)2+H2↑.
 实验室配制500mL、0.2mol/L的Na2SO4溶液,实验操作步骤有:
实验室配制500mL、0.2mol/L的Na2SO4溶液,实验操作步骤有: