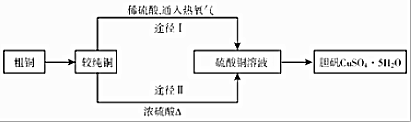
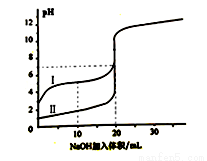
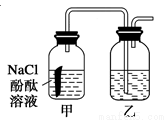
题目内容
11.a、b、c是同周期的三种短周期元素.a的原子结构示意图为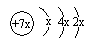 ,b与c形成的化合物的电子式为
,b与c形成的化合物的电子式为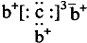 ,下列比较中正确的是( )
,下列比较中正确的是( )| A. | 原子半径:a>b>c | B. | 非金属性:a>c | ||
| C. | 氢化物的稳定性:c>a | D. | 最高价含氧酸的酸性:c>a |
分析 a的原子结构示意图为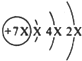 ,第一电子层容纳2个电子,故x=2,a的质子数为14,故a为Si元素;b与c形成化合物的电子式为
,第一电子层容纳2个电子,故x=2,a的质子数为14,故a为Si元素;b与c形成化合物的电子式为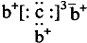 ,则b处于ⅠA族、c处于ⅤA族,a、b、c同周期,故b为Na元素,则c为P元素,以此来解答.
,则b处于ⅠA族、c处于ⅤA族,a、b、c同周期,故b为Na元素,则c为P元素,以此来解答.
解答 解:A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,则原子半径Na>Si>P,故A错误;
B.同周期元素从左到右元素的非金属性逐渐增强,P>Si,故B错误;
C.非金属性P>Si,元素的非金属性越强,对应的氢化物越稳定,故C正确;
D.非金属性越强最高价含氧酸的酸性越强,非金属性P>Si,故最高价含氧酸的酸性c>a,故D正确.
故选CD.
点评 本题考查原子结构与元素周期率,为高频考点,侧重考查核外电子排布规律、结构性质位置关系、元素周期律、物质的性质等,难度中等,注意根据原子结构示意图与电子式推断元素.

练习册系列答案
相关题目
2.下列说法不正确的是( )
| A. | 使用滴定管前要检查是否漏液 | |
| B. | 用简易量热计测定反应热时,用环形玻璃搅拌棒进行搅拌使酸和碱充分反应,以达到良好的实验效果 | |
| C. | 用精密pH试纸测得某浓度氯水的pH为3.5 | |
| D. | 燃料电池实验中,用KNO3溶液或Na2SO4溶液代替蒸馏水,效果要好得多 |
6.同温同压下,燃烧20mLH2S用去O225mL,则充分燃烧的H2S与不充分燃烧的H2S的质量之比为( )
| A. | 1:2 | B. | 2:3 | C. | 3:1 | D. | 3:2 |
16.下列说法中错误的是( )
| A. | ${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、H+和H2是氢元素的四种不同粒子 | |
| B. | ${\;}_{20}^{40}$Ca和${\;}_{20}^{42}$Ca、石墨和金刚石均互为同素异形体 | |
| C. | ${\;}_{1}^{1}$H和${\;}_{1}^{2}$H是不同的核素 | |
| D. | 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同 |
3.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,11.2L CHCl3含有的原子总数为2.5NA | |
| B. | 25g质量分数为68%的H2O2溶液中含有氧原子数目为NA | |
| C. | 高温下,16.8gFe与足量水蒸气完全反应失去0.8NA个电子 | |
| D. | 1molCH5+中含有的电子数目为11NA |