题目内容
结构决定性质:如最外层电子数决定元素性质,“官能团”是决定有机物性质的原子或原子团.下列原子团不是有机“官能团”的是( )
| A、-CH3 |
| B、-CHO |
| C、-COOH |
| D、-OH |
考点:烃的衍生物官能团
专题:有机化学基础
分析:常见官能团有羟基、氨基、羧基、醛基、酯基等,烃基不属于官能团.
解答:
解:官能团决定有机物的主要性质,题中-OH、-CHO、-COOH都是官能团,-CH3为烃基,不是官能团.
故选A.
故选A.
点评:本题考查有机物的官能团的判断,题目难度不大,注意把握常见有机物的官能团的种类、结构和性质,注意苯环、烃基不是官能团.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
在密闭容器中发生可逆反应4NH3+5O2?4NO+6H2O(g),以下是不同情况下的反应速率,其中最快的是( )
| A、v(O2)=0.01 mol?L-1?s-1 |
| B、v(NH3)=0.02 mol?L-1?s-1 |
| C、v(H2O)=0.04 mol?L-1?s-1 |
| D、v(NO)=0.03 mol?L-1?s-1 |
下列有关说法正确的是( )
| A、Na2O2能与水反应,所以Na2O2可以作气体的干燥剂 |
| B、溴化银具有感光性,碘化银不具有感光性,但AgI可用于人工降雨 |
| C、碘易溶于酒精,所以可用酒精从碘水中萃取碘单质 |
| D、钠很活泼,故钠应保存在石蜡或煤油中 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、1.0mol?L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- |
| B、含有大量Fe2+的溶液中:H+、Mg2+、ClO-、NO3- |
| C、c(H+)=10-12mol?L-1的溶液:K+、Ba2+、Cl-、Br- |
| D、能使Al溶解产生H2的溶液中:NH4+、Na+、SiO32-、HCO3- |
设为阿伏加德罗常数,下列说法中正确的是( )
| A、2.4g金属镁与足量盐酸完全反应,失电子总数为0.2NA |
| B、2NA个二氧化碳分子的质量为44g |
| C、0.1mol/L NaCl溶液中,Na+与Cl-离子总数为0.2NA |
| D、17g氨气中所含原子数为NA |
下列各组热化学方程式中,△H1>△H2的是( )
A、C(s)+O2(g)═CO2(g)△H1 C(s)+
| ||
| B、S(g)+O2(g)═SO2(g)△H1 S(s)+O2(g)═SO2(g)△H2 | ||
C、2H2(g)+O2(g)═2H2O(l)△H1 H2(g)+
| ||
| D、CaCO3(s)═CaO(s)+CO2(g)△H1 CaO(s)+H2O(l)═Ca(OH)2(s)△H2 |
在加热条件下,过量铁与浓硝酸发生反应的化学方程式为:Fe+4HNO3(浓)
Fe(NO3)2+2NO2↑+2H2O下列有关该反应的说法中,正确的是( )
| ||
| A、浓HNO3是还原剂,NO2是还原产物 |
| B、氧化性:浓HNO3>Fe(NO3)2 |
| C、氧化剂与还原剂的物质的量之比为4:1 |
| D、若反应产生了0.1mol NO2,转移的电子数为0.2NA |
深秋雨后的清晨,我们常会遇到大雾天气,雾中小液滴直径范围是( )
| A、小于1 nm |
| B、在1~100 nm间 |
| C、大于100 nm |
| D、无法确定 |
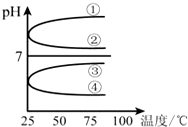 (1)稀释0.1mol?L-1氨水时,随着水量的增加而减小的是
(1)稀释0.1mol?L-1氨水时,随着水量的增加而减小的是