题目内容
反应2KMnO4+16HCl═2MnCl2+2KCl+5Cl2↑+8H2O中,MnCl2易溶于水且易电离.
(1)还原剂是 ,氧化产物是 (填化学式).
(2)氧化剂、还原剂的物质的量之比
(3)将上述化学方程式改写成离子方程式: .
(4)用单线桥(或双线桥)标出电子转移的方向和数目
2KMnO4+16HCl═2MnCl2+2KCl+5Cl2↑+8H2O.
(1)还原剂是
(2)氧化剂、还原剂的物质的量之比
(3)将上述化学方程式改写成离子方程式:
(4)用单线桥(或双线桥)标出电子转移的方向和数目
2KMnO4+16HCl═2MnCl2+2KCl+5Cl2↑+8H2O.
考点:氧化还原反应,氧化还原反应的电子转移数目计算
专题:
分析:2KMnO4+16HCl═2MnCl2+2KCl+5Cl2↑+8H2O中,Mn元素的化合价降低,Cl元素的化合价升高,以此来解答.
解答:
解:(1)2KMnO4+16HCl═2MnCl2+2KCl+5Cl2↑+8H2O中,Cl元素的化合价升高,HCl为还原剂,失去电子被氧化,则Cl2为氧化产物,
故答案为:HCl;Cl2;
(2)由反应可知,2mol氧化剂与10mol还原剂转移电子相等,则氧化剂、还原剂的物质的量之比为1:5,故答案为:1:5;
(3)该反应中只有氯气、水在离子反应中保留化学式,则离子反应为2MnO4-+16H++10Cl-═2Mn2++Cl2↑+8H2O,
故答案为:2MnO4-+16H++10Cl-═2Mn2++Cl2↑+8H2O;
(4)反应2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中化合价降低的Mn元素所在的反应物KMnO4是氧化剂,化合价升高的Cl元素所在的反应物HCl是还原剂,对应的产物MnCl2是还原产物,Cl2是氧化产物,可转移电子10e-,表示方法为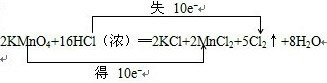 ,
,
故答案为: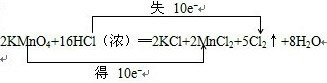 .
.
故答案为:HCl;Cl2;
(2)由反应可知,2mol氧化剂与10mol还原剂转移电子相等,则氧化剂、还原剂的物质的量之比为1:5,故答案为:1:5;
(3)该反应中只有氯气、水在离子反应中保留化学式,则离子反应为2MnO4-+16H++10Cl-═2Mn2++Cl2↑+8H2O,
故答案为:2MnO4-+16H++10Cl-═2Mn2++Cl2↑+8H2O;
(4)反应2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中化合价降低的Mn元素所在的反应物KMnO4是氧化剂,化合价升高的Cl元素所在的反应物HCl是还原剂,对应的产物MnCl2是还原产物,Cl2是氧化产物,可转移电子10e-,表示方法为
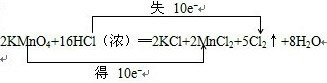 ,
,故答案为:
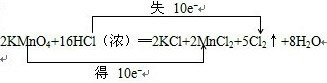 .
.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,题目难度不大.

练习册系列答案
相关题目
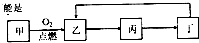 甲~丁是含同一种元素的四种物质,甲和丁分别是该元素的单质和最高价氧化物的水化物,它们之间有如图所示的转化关系,甲不可能是( )
甲~丁是含同一种元素的四种物质,甲和丁分别是该元素的单质和最高价氧化物的水化物,它们之间有如图所示的转化关系,甲不可能是( )| A、Fe | B、Si | C、Al | D、S |
下列反应中,不属于氧化还原反应的是( )
| A、锌和硫酸反应:Zn+H2SO4═ZnSO4+H2 |
| B、碳酸钙和盐酸反应:CaCO3+2HCl═CaCl2+CO2+H2O |
| C、亚硫酸和双氧水反应:H2SO3+H2O2═H2SO4+H2O |
| D、铁和硫酸铜溶液反应:Fe+CuSO4═FeSO4+Cu |
NA为阿伏加德罗常数,下列有关说法中不正确的是( )
| A、标准状况下,22.4 L氦气含有NA个氦原子 |
| B、20 g重水含有10 NA个电子 |
| C、12.5 mL l6 mol?L-1浓硫酸与足量铜反应,转移电子数为0.2 NA |
| D、1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1 NA |