题目内容
15.下列有关“氢化锂三兄弟”--LiH、LiD、LiT的叙述中正确的是( )| A. | 三种物质质子数之比为1:2:3 | B. | 三种物质中子数之比为1:1:1 | ||
| C. | 三种物质的摩尔质量之比为8:9:10 | D. | 三种物质的化学性质不同 |
分析 Li的质子数为3,H、D、T指氢的同位素11H、12H、13H,H、D、T的质子数都是1,中子数分别为0、1、2,质量数=质子数+中子数,质量数之比等于摩尔质量之比,利用组成和结构来分析物质的化学性质.
解答 解:Li的质子数为3,H、D、T指氢的同位素11H、12H、13H,H、D、T的质子数都是1,中子数分别为0、1、2.
A.LiH、LiD、LiT的质子数之比为(3+1):(3+1):(3+1)=1:1:1,故A错误;
B.LiH、LiD、LiT的中子数之比为(4+0):(4+1):(4+2)=4:5:6,故B错误;
C.LiH、LiD、LiT的摩尔质量之比为(7+1):(7+2):(7+3)=8:9:10,故C正确;
D.LiH、LiD、LiT的组成元素相同,结构相同,则三种物质的化学性质相同,故D错误;
故选C.
点评 本题考查原子的构成、物质的组成及原子中的数量关系,选项C、D都是解答中的易错点,题目难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
5.下列含有共价键的化合物是( )
| A. | HI | B. | NaOH | C. | Br2 | D. | NaCl |
3.元素的性质随原子序数的递增呈周期性变化的原因是( )
| A. | 元素原子的电子层数呈周期性变化 | |
| B. | 元素原子的核外电子排布呈周期性变化 | |
| C. | 元素的化合价呈周期性变化 | |
| D. | 元素原子半径呈周期性变化 |
20.下列原子或离子的电子排布的表示方法中,违反洪特规则的是( )
①Ca2+:1s22s22p63s23p6
②F-:1s22s23p6
③P: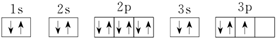
④Cr:1s22s22p63s23p63d44s2
⑤Fe:1s22s22p63s23p63d64s2
⑥Mg2+:1s22s22p6
⑦C: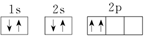
①Ca2+:1s22s22p63s23p6
②F-:1s22s23p6
③P:

④Cr:1s22s22p63s23p63d44s2
⑤Fe:1s22s22p63s23p63d64s2
⑥Mg2+:1s22s22p6
⑦C:

| A. | ①③⑥ | B. | ②④⑦ | C. | ③④⑥ | D. | ③④⑦ |
4.要证明某溶液中不含有Fe3+,而可能含有Fe2+,合理顺序是( )
①加入足量氯水 ②取少量试液 ③加入少量KSCN溶液.
①加入足量氯水 ②取少量试液 ③加入少量KSCN溶液.
| A. | ①③② | B. | ①②③ | C. | ②③① | D. | ②①③ |



 .
.