题目内容
13.短周期金属元素甲~戊在元素周期表中的相对位置如下表所示.下列判断正确的是( )| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A. | 原子半径:丙<丁<戊 | B. | 金属性:甲<丙 | ||
| C. | 氢氧化物的碱性:丙>丁>戊 | D. | 最外层电子数:甲>乙 |
分析 由短周期金属元素甲~戊在元素周期表中的相对位置,可知甲为Li、乙为Be、丙为Na、丁为Mg、戊为Al.
A.同周期自左而右原子半径减小;
B.同主族自上而下金属性增强;
C.同周期自左而右金属性减弱,金属性越强,最高价氧化物对应水化物的碱性越强;
D.同周期自左而右主族元素最外层电子数增大.
解答 解:由短周期金属元素甲~戊在元素周期表中的相对位置,可知甲为Li、乙为Be、丙为Na、丁为Mg、戊为Al.
A.同周期自左而右原子半径减小,故原子半径:丙>丁>戊,故A错误;
B.同主族自上而下金属性增强,故金属性:甲<丙,故B正确;
C.同周期自左而右金属性减弱,故金属性:丙>丁>戊,金属性越强,最高价氧化物对应水化物的碱性越强,故C正确;
D.同周期自左而右主族元素最外层电子数增大,最外层电子数:甲<乙,故D错误,
故选:BC.
点评 本题考查元素周期表与元素周期律,侧重对元素周期律的可知,需要学生熟练掌握短周期元素.

练习册系列答案
相关题目
18.下列有关有机物结构的叙述不正确的是( )
| A. | 一氟一氯甲烷只有一种结构,可以证明甲烷是正四面体结构而不是平面正方形结构 | |
| B. | 乙烯和甲苯分子中所有原子都在同一个平面上 | |
| C. | 邻二甲苯没有同分异构体表明苯的凯库勒结构式存在局限,不准确 | |
| D. | 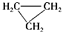 和CH3-CH═CH2互为同分异构体 和CH3-CH═CH2互为同分异构体 |
19.下列有关同位素叙述正确的是( )
| A. | ${\;}_{6}^{12}C$、${\;}_{6}^{13}C$、${\;}_{6}^{14}C$及金刚石、石墨都是碳的同位素 | |
| B. | 同位素的原子的物理性质、化学性质相同 | |
| C. | 同位素原子的本质区别在于质量数不同 | |
| D. | 质子数相同,中子数不同的原子互为同位素 |
1.下列化学用语表示正确的是( )
| A. | 水的电子式:H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2-H+ | |
| B. | 乙烷的结构简式:C2H6 | |
| C. | 铝的原子结构示意图: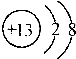 | |
| D. | 硫酸钠的电离方程式:Na2SO4═2Na++SO42- |
8.将新制氯水分别滴入下列溶液中,由实验现象得出的结论正确韵是( )
| 选项 | 氯水滴入下列溶液中 | 实验现象 | 结论 |
| A | 滴有KSCN的FeC12溶液 | 变红 | C12具有还原性 |
| B | 滴有石蕊的NaOH溶液 | 褪色 | C12具有酸性 |
| C | 紫色石蕊溶液 | 先变红后褪色 | C12具有漂白性 |
| D | KI淀粉溶液 | 变蓝 | C12具有氧化性 |
| A. | A | B. | B | C. | C | D. | D |
5.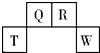 短周期元素T、Q、R、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族族序数相等.它们的最高价氧化物的水化物依次为甲、乙、丙、丁.下列叙述不正确的是( )
短周期元素T、Q、R、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族族序数相等.它们的最高价氧化物的水化物依次为甲、乙、丙、丁.下列叙述不正确的是( )
 短周期元素T、Q、R、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族族序数相等.它们的最高价氧化物的水化物依次为甲、乙、丙、丁.下列叙述不正确的是( )
短周期元素T、Q、R、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族族序数相等.它们的最高价氧化物的水化物依次为甲、乙、丙、丁.下列叙述不正确的是( )| A. | R的氢化物可以既有极性键又有非极性键 | |
| B. | 常温下丁的浓溶液可用T单质所制的容器来盛装 | |
| C. | 丁的浓溶液与Q的单质加热发生反应,可生成体积比为1:2的两种气体 | |
| D. | 甲、乙、丙、丁受热均易分解 |
2.下列有关化学用语或表达正确的是( )
| A. | 三硝酸纤维素脂 | B. | 硬酯酸钠 | ||
| C. | 硝酸苯的结构简式: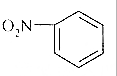 | D. | NaCl晶体模型: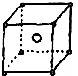 |
3.下列化学方程式或离子方程式正确的是( )
| A. | 将Al条投入NaOH溶液中:Al+OH-+H2O═[Al(OH)4]-+H2↑ | |
| B. | 向氯化铵的稀溶液中加入少量NaOH NH4++OH-═NH3↑+H2O | |
| C. | 浓盐酸与铁屑反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 向浓硝酸中加入铜片Cu+4H++2N03-═Cu2++2NO2↑+2H2O |
