题目内容
13.B和D是生活中的两种常见的金属单质,A是红棕色的金属氧化物,J是一种难溶于水的白色化合物,受热后容易发生分解.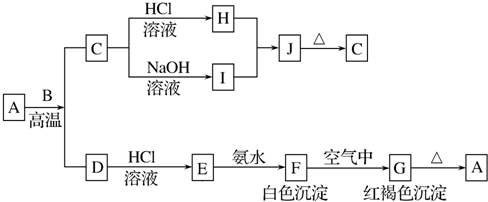
(1)A的化学式是Fe2O3,B的化学式是Al
(2)F在空气中转化为G的化学方程式:4Fe(OH)2+O2+2H2O═4Fe(OH)3
(3)C转化为I的离子方程式:Al2O3+2OH-═2AlO2-+H2O
(4)J转化为C的化学方程式:2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O
(5)A与B反应的化学方程式:4Al+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+2Al2O3.
分析 A是一种红棕色金属氧化物,则A为Fe2O3,A和金属B在高温下发生铝热反应,生成的C为Al2O3,既能和酸反应又能和碱反应,则金属B是铝,H是氯化铝,I是偏铝酸钠,J是一种难溶于水的白色化合物为氢氧化铝,J为Al(OH)3;D为Fe,结合白色沉淀在空气中变成红褐色沉淀,可知为氢氧化亚铁和氢氧化铁之间的转换,则G是Fe(OH)3,F是Fe(OH)2,E是FeCl2,然后结合物质的性质及化学用语来解答.
解答 解:A是一种红棕色金属氧化物,则A为Fe2O3,A和金属B在高温下发生铝热反应,生成的C为Al2O3,既能和酸反应又能和碱反应,则金属B是铝,H是氯化铝,I是偏铝酸钠,J是一种难溶于水的白色化合物为氢氧化铝,J为Al(OH)3;D为Fe,结合白色沉淀在空气中变成红褐色沉淀,可知为氢氧化亚铁和氢氧化铁之间的转换,则G是Fe(OH)3,F是Fe(OH)2,E是FeCl2,
(1)由上述分析可知,A、B分别为Fe2O3、,故答案为:Fe2O3;Al;
(2)F在空气中转化为G的化学方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(3)C转化为I的离子方程式为Al2O3+2OH-═2AlO2-+H2O,故答案为:Al2O3+2OH-═2AlO2-+H2O;
(4)J转化为C的化学方程式为2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O,故答案为:2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O;
(5)A与B反应的化学方程式为4Al+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+2Al2O3,故答案为:4Al+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+2Al2O3.
点评 本题考查无机物的推断,为高频考点,把握物质的颜色、沉淀的判断、Al和Fe的化合物性质等为解答的关键,侧重分析与推断能力的考查,注意J、A为推断的突破口,题目难度不大.

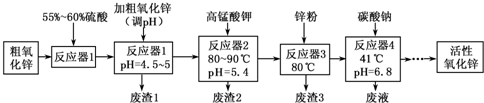
| Fe(OH)2 | Fe( OH)3 | Cu(OH)2 | Zn(OH)2 | Mn(OH)2 | |
| 开始沉淀的pH | 7.5 | 2.2 | 5.2 | 6.4 | 8.6 |
| 沉淀完全的pH | 9.0 | 3.2 | 6.7 | 8.0 | 10.1 |
(1)“废渣1”的主要成分是Fe( OH)3.
(2)完成“反应器2”中反应之一的离子方程式:□MnO-4+□Mn2++□2H2O=□MnO2↓+□H+
(3)蘸取“反应器2”中的溶液点在淀粉碘化钾试纸上,如果观察到试纸变蓝,说明KMnO4过量.
(4)“废渣2”分离出的MnO2可用于制取MnO,已知:
2MnO2(s)+C(s)═2MnO(s)+CO2(g)△H=-174.6kJ•mol-1
C(s)+CO2(g)═2CO(g)△H=+283.0kJ•mol-1
试写出MnO2(s)与CO(g)反应制取MnO(s)的热化学方程式:MnO2(s)+CO(g)=MnO(s)+CO2(g)△H=-228.8kJ/mol.
(5)“反应器3”中加入锌粉的作用是调节溶液pH,除去溶液中Cu2+.
(6)“反应器4”得到的废液中,含有的主要离子除了Na+外,还有K+、SO42-.
(7)从“反应器4”中经过滤等操作得到碱式碳酸锌.取碱式碳酸锌3.41g,在400~450℃下加热至恒重,得到ZnO 2.43g和标准状况下CO2 0.224L,碱式碳酸锌的化学式ZnCO3•2Zn(OH)2•H2O.

| A. | 拉瓦锡研究了空气的成分,让大家认识了氧气 | |
| B. | 图为雾霾的主要成分示意图,汽车尾气的大量排放是造成雾霾天气的人为因素之一 | |
| C. | “滴水石穿、绳锯木断、落汤螃蟹着红袍”均不包含化学变化 | |
| D. | “看似风平浪静,实则暗流涌动”形象地描述了溶解平衡的状态 |
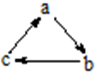 下列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
下列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )| a | b | c | |
| A | Al | AlCl3 | Al(OH)3 |
| B | HCl | H2CO3 | HClO |
| C | Si | SiO2 | H2SiO3 |
| D | NaOH | NaHCO3 | Na2CO3 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 | |
| B. | 分子组成相差一个或几个CH2原子团的化合物必定互为同系物 | |
| C. | 同系物的分子量数值一定相差14的整数倍 | |
| D. | 同系物的化学性质相似,物理性质随碳原子数的递增呈现规律性变化 |
| A. | pH=4 | B. | c(H+)=0.001 mol•L-1 | ||
| C. | c(OH- )=1×10-11 mol•L-1 | D. | c(H+):c(OH- )=1×104 |
| A. | 任何晶体中都存在化学键 | |
| B. | 固体SiO2一定是晶体 | |
| C. | 晶体的自范性是晶体中粒子在微观空间里呈现周期性的有序排列的宏观表象 | |
| D. | X-射线衍射法是区分晶体和非晶体的唯一方法 |
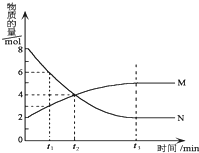 在一定温度下,在某密闭容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示.下列叙述中,正确的是( )
在一定温度下,在某密闭容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示.下列叙述中,正确的是( )| A. | 该反应的化学方程式为M═2N | |
| B. | 若t1=1,则反应开始至t1时间段M 的反应速率为1mol﹒L-1﹒min-1 | |
| C. | t2时正逆反应速率相等,反应达到平衡状态 | |
| D. | t3时正反应速率等于逆反应速率 |

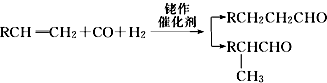
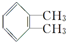 ,名称为邻二甲苯.
,名称为邻二甲苯.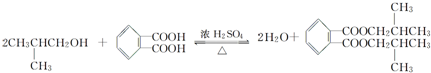 .
.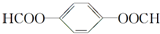 ; 1molX与NaOH溶液共热反应,最多消耗4molNaOH.
; 1molX与NaOH溶液共热反应,最多消耗4molNaOH.