题目内容
7.从柑橘中提取得到结构简式如图所示的化合物,则下列有关它的推断错误的是( )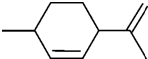
| A. | 属于芳香烃,分子式为C10H16 | B. | 常温下呈液态,比水轻 | ||
| C. | 其一氯代物有8种(不考虑顺反异构) | D. | 能与溴水发生加成反应 |
分析 由结构简式可知分子式,分子中含2个双键,结合烯烃的性质来解答.
解答 解:A.由结构简式可知分子式为C10H16,故A正确;
B.烃类密度都比小,相对分子质量较大,常温下呈液态,故B正确;
C.分子结构不对称,含9种位置的H,则一氯代物有9种,故C错误;
D.含双键,则能与溴水发生加成反应,故D正确;
故选C.
点评 本题考查有机物的结构和性质,为高频考点,把握有机物的官能团与物质性质的关系为解答的关键,侧重烯烃性质及一氯代物的考查,题目难度不大.

练习册系列答案
 目标测试系列答案
目标测试系列答案
相关题目
5.下列说法正确的是( )
| A. | 16gO2所含的分子数为6.02×1023个 | |
| B. | 0.5molH2SO4含有的原子数目为3.5NA | |
| C. | 18gH2O中原子的物质的量为1mol | |
| D. | 22g物质A中含有分子数为3.01×1023,则A的摩尔质量为44g |
15.下列有关说法正确的是( )
| A. | 反应2Mg(s)+CO2(g)═C(s)+2MgO(s)能自发进行,则该反应的△H>0 | |
| B. | 电解法精炼铜时,粗铜作阳极,精铜作阴极 | |
| C. | 在硫酸钡悬浊液中加入足量饱和Na2CO3溶液处理,向所得沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3) | |
| D. | CH3COOH溶液加水稀释后,电离度增大,溶液中$\frac{C(C{H}_{3}CO{O}^{-})C({H}^{+})}{C(C{H}_{3}COOH)}$的值不变 |
2.饮水安全在人们生活中占有极为重要的地位,某研究小组提取三处被污染的水源进行了分析,给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质.A、B、C、D、E五种常见化合物都是由下表中的离子形成:
为了鉴别上述化合物,分别进行以下实验,其结果如下所示:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃片);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)写出A、B、C、D、E的化学式:A:NaHCO3、B:KNO3、C:KAl(SO4)2、D:CuSO4 E:NaOH
(2)将含1mol A的溶液与含1mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为Na2CO3.
(3)写出实验②发生反应的离子方程式:Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═[Al(OH)4]-.
(4)C常用作净水剂,用离子方程式表示其净水原理:Al3++3H2O?Al(OH)3(胶体)+3H+.
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 | SO42- HCO3- NO3- OH- |
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃片);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)写出A、B、C、D、E的化学式:A:NaHCO3、B:KNO3、C:KAl(SO4)2、D:CuSO4 E:NaOH
(2)将含1mol A的溶液与含1mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为Na2CO3.
(3)写出实验②发生反应的离子方程式:Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═[Al(OH)4]-.
(4)C常用作净水剂,用离子方程式表示其净水原理:Al3++3H2O?Al(OH)3(胶体)+3H+.
16.H2和 I2在一定条件下能发生反应:H2(g)+I2(g)?2HI(g)△H=-a kJ/mol.已知:

(a、b、c 均大于零).下列说法正确的是( )

(a、b、c 均大于零).下列说法正确的是( )
| A. | H2、I2和 HI 分子中的化学键都是非极性共价键 | |
| B. | 断开 2 mol HI 分子中的化学键所需能量约为(c+b+a) kJ | |
| C. | 相同条件下,1 mol H2(g)和 1mol I2(g)总能量小于 2 mol HI (g)的总能量 | |
| D. | 向密闭容器中加入 2 mol H2(g)和 2 mol I2(g),充分反应后放出的热量为 2a kJ |
17.常温下,下列溶液中的微粒浓度关系正确的是( )
| A. | pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| B. | 0.1mol•L-1的Na2CO3溶液:c(OH-)=c(H+)+c(HCO3-)+c(CO32-) | |
| C. | 向0.2mol•L-1NaHCO3溶液中加入等体积0.1mol•L-1NaOH溶液:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-) | |
| D. | 常温下,CH3COOH)和CH3COONa混合溶液【PH=7,c(Na+)=0.1mol•L-1】:c(CH3COO-)=0.1mol•L-1 |